11月13日,普米斯生物技术公司(以下简称“普米斯”),宣布与BioNTech达成股权收购协议。
根据协议条款,BioNTech将以8亿美元(约57.81亿元人民币)预付款收购普米斯100%已发行股本(可根据惯例对收购价格进行调整),支付方式主要为现金和部分美国存托股份(ADS)。此外,BioNTech将在普米斯达到双方约定的里程碑条件时,额外支付最高1.5亿美元(约10.84亿元人民币)的里程碑付款。该交易预计于2025年*季度完成,具体取决于按惯例完成交割条件和监管部门的批准。
本次交易完成后,BioNTech将获得普米斯候选药物管线及其双特异性抗体药物开发平台的全部权利,进一步扩大其在中国的业务范围;普米斯珠海将作为BioNTech中国研发中心开展相关R&D研究;符合国际标准的普米斯南通生产基地将为BioNTech未来的全球产品生产和供应做出贡献;逾300名普米斯研发、生产和支持职能部门员工加入BioNTech。
01.
与普米斯合作的双抗表现优异
此次并购建立在双方去年两次合作之上。
2023年7月,BioNTech与普米斯生物达成过战略研究合作、项目引进选择以及全球许可协议。根据该协议条款,BioNTech将获得普米斯用于治疗恶性肿瘤的一款临床前研究阶段双特异性抗体和一款临床研究阶段单克隆抗体的全球*选择权。此外,普米斯将多个在研临床前纳米抗体项目专属授权给BioNTech,并根据其需求提供指定靶向纳米抗体开发服务。
短短四个月后,双方再次达成合作。BioNTech以5500万美元的首付款,及超10亿美元的开发、注册和商业里程碑付款以及分级销售提成,获得普米斯抗PD-L1/VEGF双特异性抗体(PM8002)在全球(大中华区除外)的开发、生产和商业化权利。
PM8002是一款双特异性抗体药物,由人源化的抗PD-L1单域抗体(VHH)融合到一个含有Fc-沉默突变的抗VEGF-A IgG1抗体上构成,现已在国内开展针对TNBC、小细胞肺癌、非小细胞肺癌、宫颈癌等多个瘤种的多项临床研究。
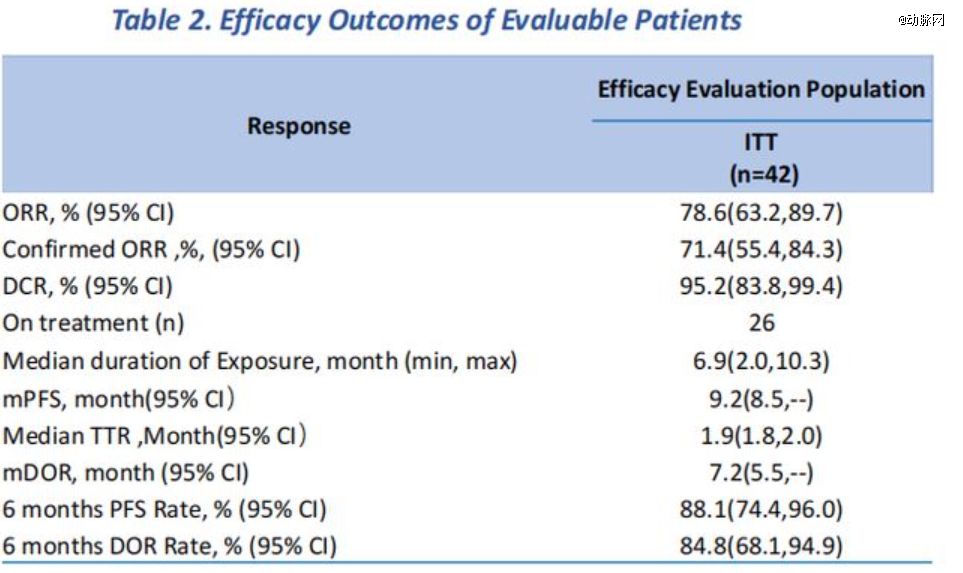
当年12月,普米斯便在第46届圣安东尼奥乳腺癌研讨会(SABCS)公布了PM8002与化疗联合治疗三阴性乳腺癌(TNBC)的疗效结果。结果显示,截至2023年6月30日,共有42例患者接受了治疗,并至少进行了一次疗效评估。药物暴露的中位持续时间为4.6个月(范围:2.0至7.6个月)。*总体ORR为78.6%(33/42),包括1例完全缓解(CR)和32例部分缓解(PR),其中29例在患者首次评估时即获得缓解。确认的ORR为71.4%,总体疾病控制率(DCR)为95.2%。中位至缓解时间(TTR)为1.9个月(95%CI:1.8~2.0)。中位目标病变*百分比变化为-47.2%(*四分位数、第三四分位数:-56.9%,-33.5%)。中位缓解持续时间(DOR)为7.2个月,中位无进展生存期(PFS)为9.2个月。
今年以来,PM8002临床进展更是喜报频传。3月,PM8002被国家药监局药品审评中心(CDE)纳入突破性治疗品种,针对适应症为联合注射用白蛋白结合型紫杉醇一线治疗不可手术的局部晚期/复发转移性三阴性乳腺癌。
4月底,PM8002获国家药品监督管理局(NMPA)批准开展一项注册性III期临床试验:PM8002注射液或安慰剂联合注射用白蛋白结合型紫杉醇一线治疗不可手术的局部晚期/复发转移性三阴性乳腺癌(TNBC)的多中心、随机、双盲III期临床研究。后又正式在Clinicaltrials.gov网站上注册了PM8002(20mg/kg Q2W)联合化疗一线治疗局部晚期或转移性三阴乳腺癌的III期临床试验。
几天后,BioNTech便宣布行使*次战略合作的全球*选择权,获得由普米斯自主研发的临床前双特异性抗体候选药物的全球开发、生产和商业化权利。
据2024年BioNTech第三季度财报披露,今年10月,BNT327/PM8002针对乳腺癌的Ⅱ期临床试验完成了首例患者给药,旨在评估该产品在两个剂量水平下与化疗联合使用,在一线和二线治疗局部晚期/转移性三阴乳腺癌(TNBC)患者的安全性、疗效和药代动力学。
小细胞肺癌方面,BioNTech宣布已于9月完成针对小细胞肺癌的Ⅱ期临床试验的首例患者给药,旨在评估BNT327/PM8002与化疗联合在未经治疗的广泛期小细胞肺癌患者中的疗效,以及在接受一线或二线治疗后进展的小细胞肺癌患者中的疗效。另一边,普米斯也在9月启动了一项III期临床,以评估PM8002联合紫杉醇对比化疗二线治疗小细胞肺癌的有效性和安全性。
02.
10条临床研究阶段管线,正着手搭建ADC技术平台
在PM8002之外,普米斯还正在推进超20个1类生物新药项目,其中多个新药项目处于临床研究阶段。公司在珠海、苏州和香港设有新药研发中心,并在上海、北京设立临床研究中心,在南通建设产业化生产基地。普米斯的核心团队拥有超过20年的高端生物新药研发、产品申报及上市经验。
从技术平台来看,普米斯在抗体发现、抗体工程改造、发现生物学、临床前、CMC研究各环节均建有核心技术平台,支持抗体新药项目从抗体发现到临床申报的全过程。
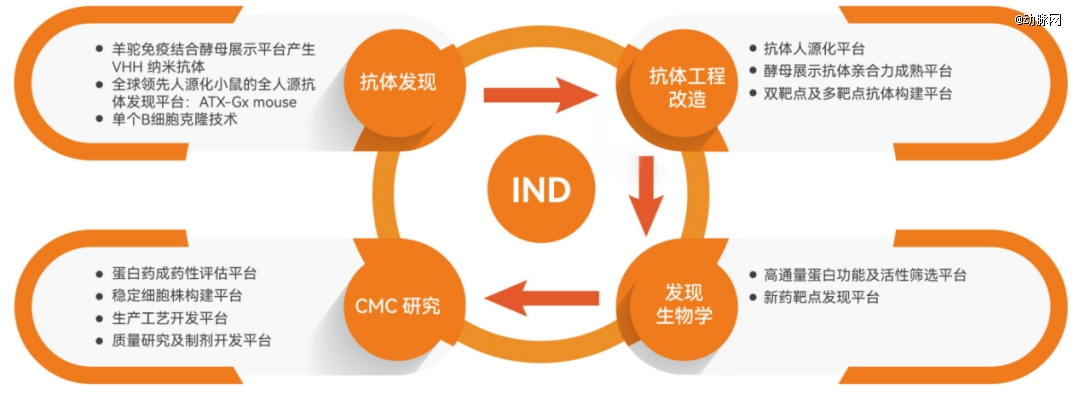
图源:普米斯官网
在候选管线方面,截至目前,普米斯已有10个抗体新药项目正处于临床研究阶段,并有多项临床试验处于Ⅱ期。
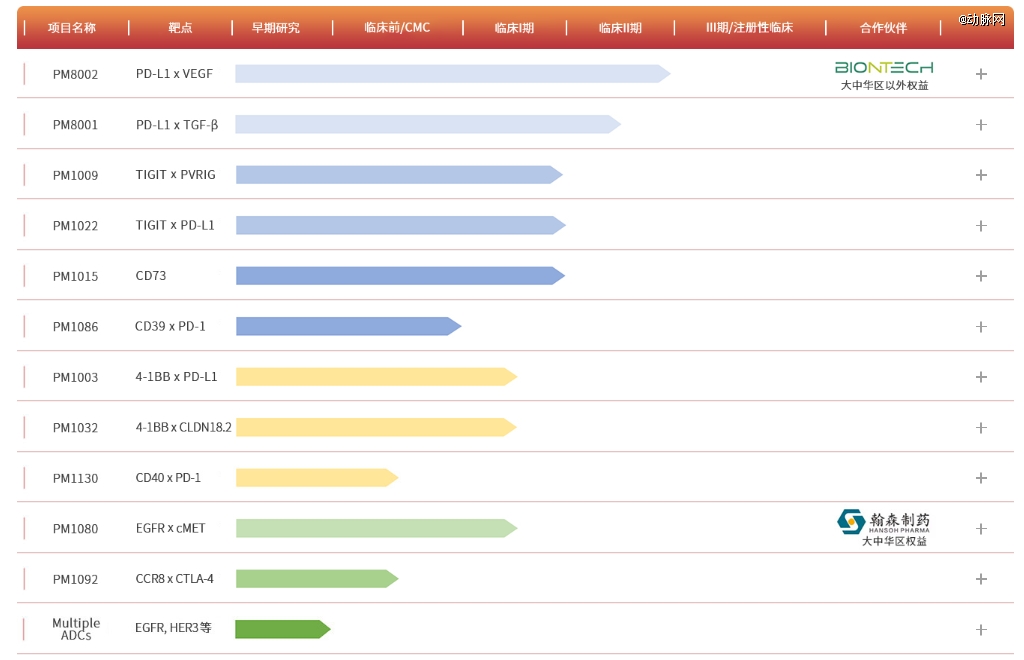
图源:普米斯官网
除与BioNTech达成合作外,普米斯还与多个药企达成战略合作。境外来看,今年年初,普米斯与美国Bitterroot Bio达成战略合作,共同研发可用于调节免疫系统和调控炎症反应的双功能蛋白类新药,从而达到治疗多种心血管疾病的效果。
国内方面,普米斯与翰森制药自2022年合作后再一次扩大战略合作关系,许可翰森制药使用普米斯自主研发的抗EGFR/cMet双特异性抗体PM1080/HS-20117用于开发抗体药物偶联物(ADC)产品,普米斯则将将获得翰森制药支付的首付款和基于ADC产品的开发、注册及基于销售的商业化里程碑潜在付款,合计不超过50亿元人民币,以及基于全球净销售额的分级特许权使用费。
而这也可以粗略视为普米斯向ADC探索的*步。这次合作中,普米斯联合创始人、董事长兼首席执行官刘晓林曾表示,此次合作将普米斯在双抗新药开发方面的优势和翰森制药的ADC开发优势结合起来,有望开发出临床效果更优的PM1080-ADC新药。
ADC是当前国产新药出海的热门品种之一,刘晓林在此前接受21世纪经济报道的采访中表示,目前普米斯已经着手搭建ADC平台,并认为“随着精准治疗时代的到来,ADC将会替代化疗,未来‘IO(肿瘤免疫疗法)+ADC’联合用药具有广阔的想象空间……下一个阶段的ADC药物开发又会回到相关抗体的生物学机制上,抗体包括单抗,双抗等的功能可能会起到更关键的作用,而抗体研发是我们的强项,普米斯有可能在这个领域发挥更多的作用。”
03.
对中国Biotech“爱不释手”的BioNTech
在去年七次牵手中国Biotech之后,对中国Biotech“爱不释手”的BioNTech不仅有“上新”还有“复购”。包括与宜联生物达成多靶点TMALIN®ADC技术平台授权协议,进一步拓展全球战略合作伙伴关系以及与3D打印药物企业三迭纪达成研究合作与平台技术许可协议等。截至目前,BioNTech已经与6家中国Biotech达成合作,多项交易金额超10亿美元。
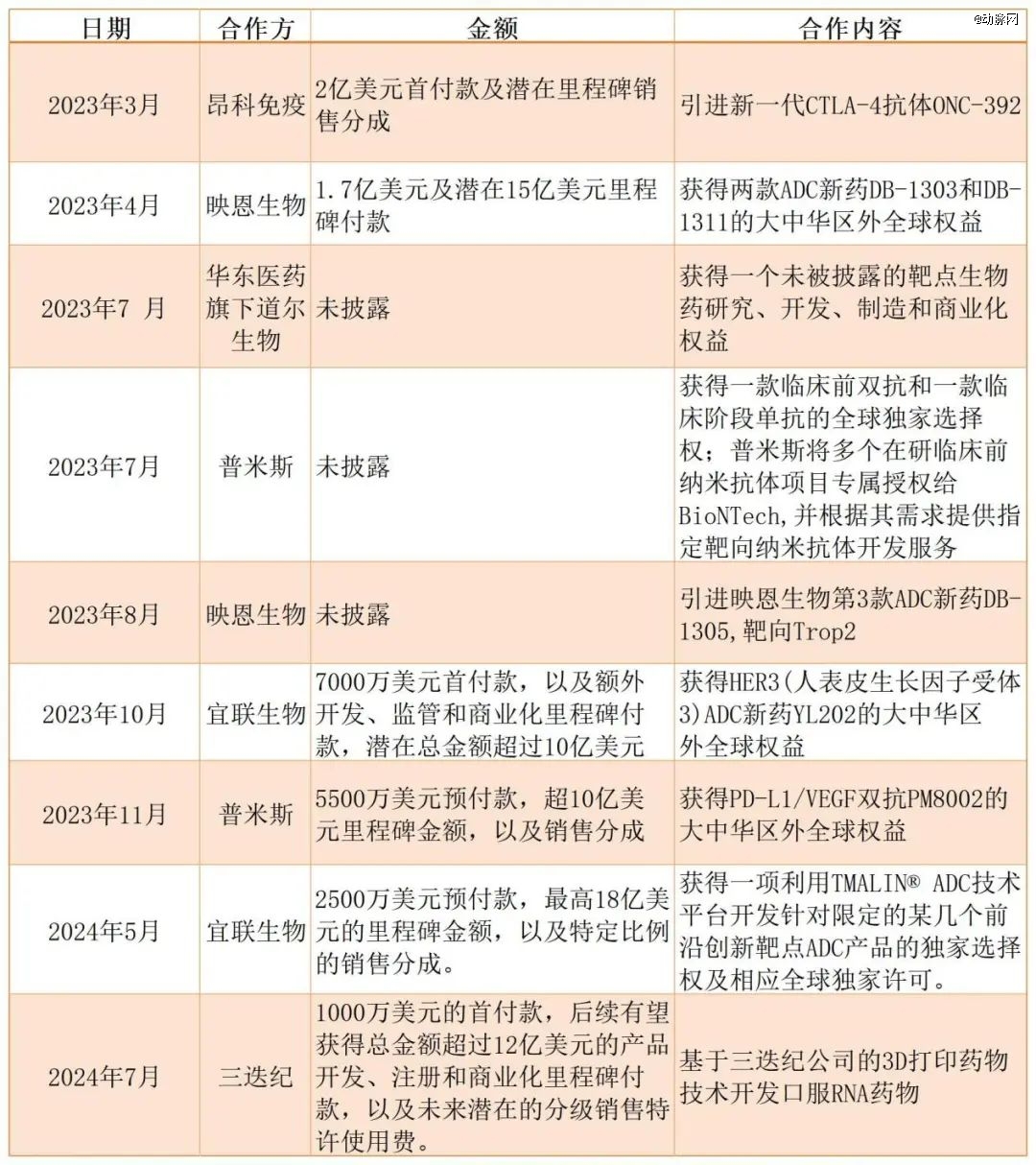
BioNTech与中国Biotech达成的BD合作(动脉新医药制图,公开信息统计,2023年至今)
而中国Biotech的表现也不辱使命,除提到普米斯的PM8002外,BioNTech的2024第三季度财报还披露了其他部分重点管线进展。
首先是与映恩生物的交易,分别是靶向HER2、B7H3、TROP2的三个ADC。
目前,靶向HER2的BNT323/DB-1303正在进行一项1/2期临床试验(NCT05150691)评估,试验对象为晚期/不可切除、复发性或转移性的HER2表达阳性实体瘤患者。一组HER2表达阳性(IHC3+,2+,1+或ISH阳性)的晚期/复发性子宫内膜癌患者已完成入组。预计将在2025年获得这一队列的数据。
此外,一项针对晚期子宫内膜癌患者的3期临床试验(NCT06340568)正在规划中。预计在2026年,公布针对HR+和HER2低表达转移性乳腺癌患者的3期临床试验的初步数据,这些患者在接受激素治疗和/或CDK4/6抑制剂治疗后出现了病情进展。
BNT324/DB-1311是靶向B7H3的ADC药物。今年7月,FDA授予BNT324/DB-1311孤儿药称号,用于治疗晚期或转移性食管鳞状细胞癌。目前正在开展一项1/2期临床试验(NCT05914116),针对晚期实体瘤患者。预计该试验的首次初步数据更新将在2024年12月的ESMO亚洲大会上展示。
在与宜联生物的合作BNT326/YL202方面,尽管今年6月一项提交给SEC的文件中透露,由于研究人员在临床试验中观察到多起死亡事件,FDA决定部分暂停该产品的1期临床试验。但目前,一项国际多中心Ⅰ期临床试验(NCT05653752)正在进行中,该试验评估BNT326/YL202作为局部晚期或转移性EGFR突变非小细胞肺癌或HR+/HER2阴性乳腺癌患者的后期线治疗。今年8月15日,FDA解除了对此试验的部分临床暂停。试验招募已重新启动,重点放在不超过3 mg/kg的剂量水平,在该剂量水平上安全状况可控,并且观察到不错的临床活性。
04.
写在最后
普米斯联合创始人、董事长兼首席执行官刘晓林曾先后在雅培、施贵宝、Adimab等公司任研发高管,也是PD-1抗体药圈内知名的科学家。公开信息显示,刘晓林2012年回国任信达生物研发副总裁一职后,“从0到1”组建并领导一支100多人的研发团队,建立了包括20多个抗体新药的产品链,并作为项目负责人领导团队成功完成国产PD-1单抗新药(信迪利单抗)的开发上市。
随后,抱着做“原始创新”的想法在珠海创办普米斯。从2018年到2024年,普米斯也曾搭上中国医药投资热潮的末班车,在资本的助力下迅速成长,后又经历了生物医药板块融资收缩,必须调整生存策略。普米斯也是无数具有新技术、新突破的中国Biotech的缩影,正如刘晓林引用20多年前再生元CEO的话说,“我们在这条路上还会犯很多错,但我们肯定会一直往前走不会死。”
参考文章:
1.BioNTech公布三季报 豪买的中国产品哪些更受重视?| *现场.研发客
2.高成长企业2024⑨丨创新药企普米斯的“中场战事”:注重原始创新,跻身全球医药竞争序列.21世纪经济报道任何使用














