一个大赔率的BD投资方向,值得投资人重视。
10月28日,艾伯维宣布以14亿美元现金收购Aliada的全部流通股权(核心管线为抗β淀粉样蛋白抗体),交易核心旨在利用Aliada的新型血脑屏障 (BBB) 穿越技术来向阿尔茨海默病(AD)等CNS疾病展开更深层次的探索。
突破血脑屏障资产的大额BD交易,近来在各类药物形式的分子都得以展现。
2024年8月,基因泰克以5000万美元预付款、短期里程碑付款及总价值19亿美元潜在里程碑获得Tau基因的锌指阻遏物和使用Sangamo Therapeutics独有的AAV衣壳STAC-BBB的权益,该AAV不仅表达出强力穿越血脑屏障(BBB)的能力,并且在广泛不同的CNS组织中STAC-BBB均能够驱动高水平的转基因表达。
小分子层面,2023年5月罗氏以“7000万美元预付款+6.1亿美元潜在里程碑”引进赞荣医药口服小分子HER2抑制剂ZN-A-1041全球权益,该分子*的特点是能够有效穿透血脑屏障,被市场认为是治疗HER2阳性乳腺癌脑转移瘤潜在最有效创新药物。
密集的BD,正在证明以突破BBB的研究方向大有可为。
01
突破血脑屏障后的广阔空间
血脑屏障最早在1895年被发现,其周密控制着中枢神经和外周循环的双向通信,其由脑微血管内皮细胞、内皮细胞紧密连接、神经胶质细胞、星形胶质细胞、周细胞、基膜等组分构成。
血脑屏障主要的功能有两个:一是通过清除代谢物和毒素来维持大脑稳态,二是提供物理屏障,防止有害分子从外周进入大脑并调节免疫运输;不过,其也限制了大部分治疗药物进入大脑内部,大量CNS治疗药物由于无法穿过BBB并在脑内达到有效治疗浓度。
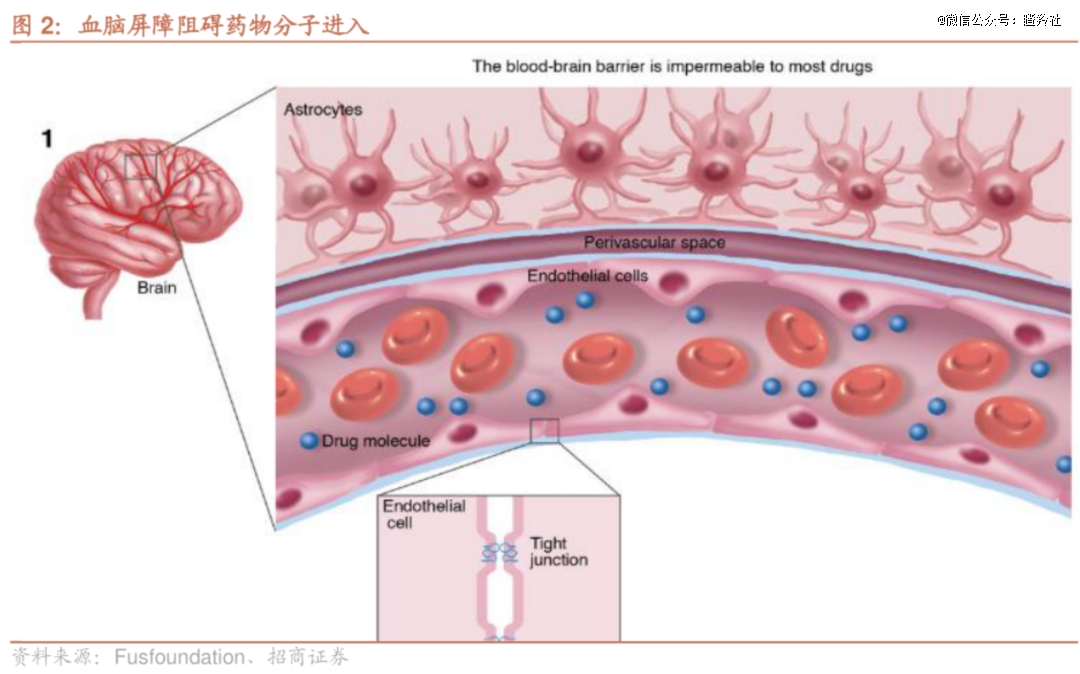
尽管血脑屏障阻挡了大部分药物分子入脑,但极少数药物分子入脑仍有几大途径:1)被动扩散:大部分小分子药物都是通过这一途径透过BBB从而实现入脑,其可能受主动外排的限制;2)通过细胞间隙入脑,该方式通常只能对一些极性低分子量的化合物适用;3)由脑内皮细胞表达的转运蛋白介导的摄取;4)由脑内皮细胞表达的受体蛋白介导的转运。
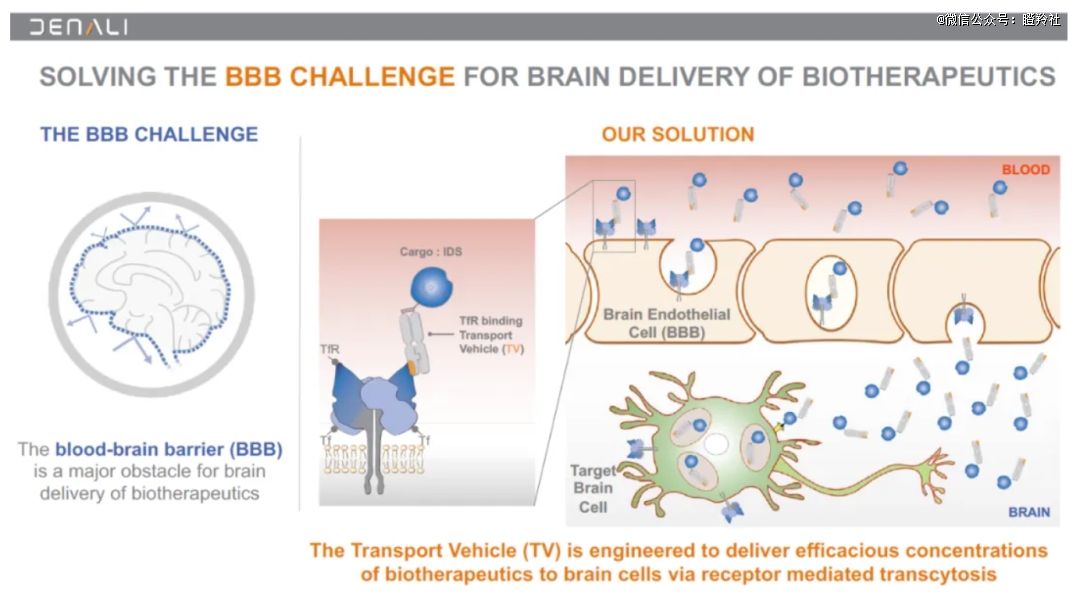
上述几种途径已经不乏一些验证性案例,以海外部分Biotech为例:Denali Therapeutics的酶替代疗法DNL310在治疗亨特综合征的1/2期临床中,其不仅能够降低大脑中与疾病相关的生物标志物水平,还表现出改善患者临床症状的初步迹象。相比过往疗效不佳的酶替代疗法,Denali公司的转运载体技术平台可具有治疗作用的大分子与能够和血脑屏障上表达的天然转运受体结合的工程化Fc片段连接在一起,将大分子递送到大脑。
另一个例子便是Angiochem公司,其开发出一个由超100种多肽结构的专有库,这些分子可以与脂蛋白受体相关蛋白(LRP-1)结合,LRP-1是参与胰岛素和生长激素等必需物质入脑的重要受体,这样的机制使得Angiochem的多肽偶联药物(PDC)能够透过BBB,进入大脑杀伤病灶。
当药物分子突破BBB之后,前途瞬间明亮起来,至少有三个大的方向可以驰骋探索:
1)CNS疾病:全球第三大疾病市场(超过10亿人饱受CNS疾病困扰),涵盖适应症种类及未满足临床需求广阔,仅以阿尔茨海默症为例,全球患病人数高达5000万人。
2)肿瘤脑转移:脑转移是癌症患者治疗预后不良的重要原因之一,如大约50%的非小细胞肺癌患者在疾病过程某个时刻会发展出脑转移、高达50%的HER2阳性转移性乳腺癌患者在病程中会发生脑转移,现如今如何增加脑转移患者的获益始终是一个难题。
3)脑肿瘤:脑部肿瘤的治疗亦是重要方向之一,如胶质母细胞瘤(GBM)是*侵袭性原发性脑肿瘤之一,病理机制复杂,极大限制了GBM传统和新型疗法的有效性,患者5年生存率仅为5%左右。
如此,投资者不难理解为何穿透BBB的技术平台和分子备受MNC的青睐。
02
已BD分子做对了什么
目前已经上市的Aβ抗体Lecanemab和Donanemab目前已经展现出强有力的有效清除β样淀粉蛋白斑块疗效,重要的改善痛点仍在于Aβ抗体这类大分子药物穿BBB入脑的效率较低,从而导致两个已商业化药物使用剂量、频率都极高,可能出现患者依从性差、注射相关不良反应多、患者负担沉重等缺点。
被艾伯维收购的Aliada首发管线为ALIA-1758,其和礼来Donanemab一样,都是靶向3位焦谷氨酸化的Aβ,不同在于其利用自家的 模块化递送平台MODEL™进行改造设计,不仅拥有潜在更好的BBB穿透效率,同时进行Fc长效改造改善过往Aβ抗体频繁注射的问题。
值得注意的是,MODEL™这项穿透BBB技术以脑内皮细胞高度表达的转铁蛋白(TfR)和CD98受体(CD98)为靶标,通过设计出高度优化的TfR或CD98粘合剂,该平台可将这些粘合剂连接在不同的“货物”上,这些货物包括治疗性抗体和siRNA等药物,其结合物可以通过转胞吞作用穿过血脑屏障进入大脑。
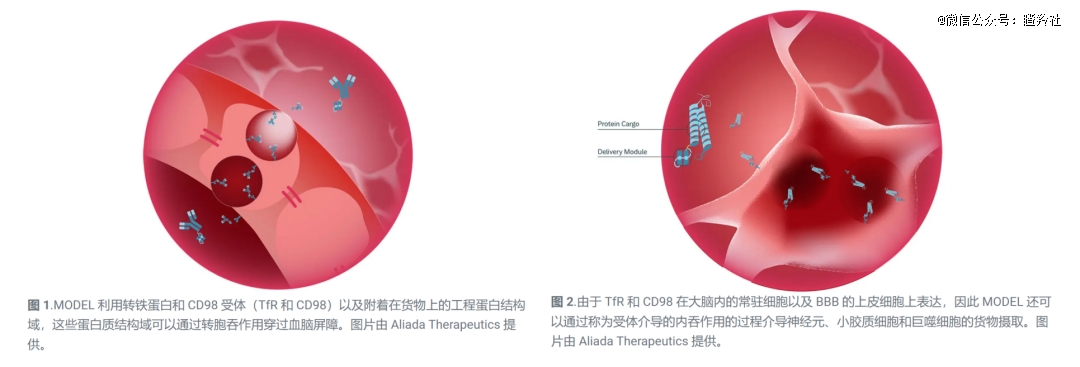
艾伯维通过这项收购,不仅宣称囊获了潜在BIC的Aβ抗体,同时还获得了MODEL™平台的使用权,为其大举押注CNS领域增强了技术储备。
另外值得一提的,便是与罗氏达成合作的赞荣医药口服小分子HER2抑制剂ZN-A-1041。
ZN-A-1041从默沙东的Tucatinib优化而来,其设计特点包括:1)高度血脑屏障通透性;2)对HER2选择性高,不良反应减少;3)在联合治疗中使用足够安全;
ZN-A-1041的潜力也在早期临床中获得验证,其在2023 ASCO大会公布HER2+脑转移乳腺癌(BCBM)数据显示,在19例至少两次肿瘤评估的脑转移乳腺癌(BCBM)患者中,ZN-1041联合卡培他滨和曲妥珠单抗的总ORR为78.9%,颅内ORR为73.7%,疾病控制率(DCR)为100%。
HER2抑制剂抑制剂作为HER2阳性乳腺癌“基药”一般的存在,赞荣医药通过提升脑透性和提升安全性照样能够获得MNC的青睐,直接印证了穿越BBB技术平台和分子的巨大价值。
03
国内难得攻坚穿透BBB技术的玩家
据业内人士介绍,由于用于筛选脑转移模型门槛较高、CDMO产业链错配、国内研发更热的大分子较小分子更难透过BBB,导致国内攻坚穿越BBB的药企较少。
从已经上市的创新药企业来说,百济神州和迪哲医药是代表性的企业。
百济神州*展现出穿越BBB潜力的分子是已经上市的PARP抑制剂帕米帕利,其在动物试验中帕米帕利就展现出比同类药物具有更强的血脑屏障穿透能力,这也促使其相比其他PARP抑制剂有更好的预防肿瘤脑转移的治疗效果。
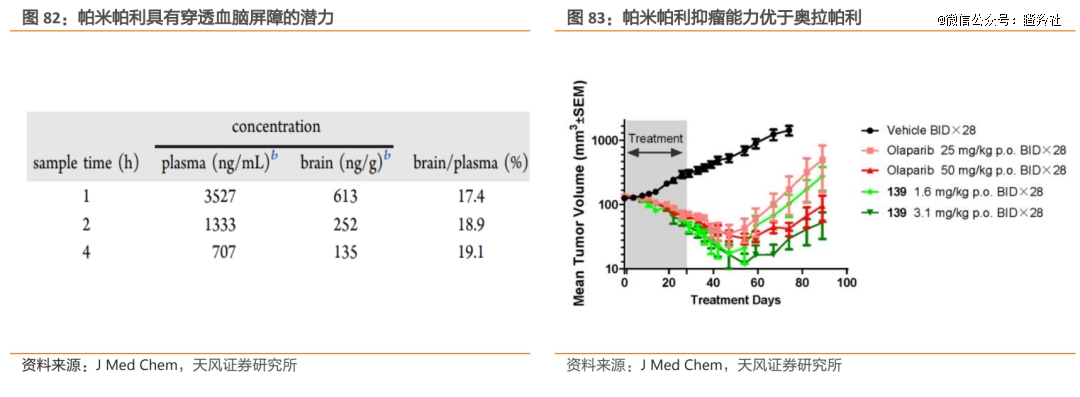
帕米帕利并不是百济神州穿越BBB技术的“独苗”,公司BGB-58067是*在中国申报临床的PRMT5抑制剂(2024年9月),其拥有较好的中枢系统渗透性和较理想的半衰期,在肺癌、胃癌和食管中具有非常好的治疗潜力。

迪哲医药是国内少有的拥有穿透血脑屏障研发技术平台的Biotech,其研发的数个可穿透血脑屏障的候选分子都具备同类*的潜力。
迪哲医药口服HER2抑制剂DZD1516是一款可透血脑屏障的HER2 TKI,已公布的DZD1516一期研究结果显示,证实了其能够完全穿透血脑屏障,且对HER2高表达的乳腺癌细胞的活性是表达野生型表皮生长因子受体(EGFR)细胞活性的300倍以上,具备高选择性。
DZD8586是迪哲医药更新自主研发能完全穿透血脑屏障的一款全新非共价LYN/BTK双靶点抑制剂,有望解决现有BTK药物耐药性问题。
DZD8586已有的针对不同血液瘤患者的I/II期临床试验数据显示,在3线治疗不同B-NHL亚型的患者中仍能取得强劲疗效,尤其在在DLBCL患者中ORR高达83.3%,并在2例中枢神经系统白血病患者中有1例获得部分缓解;在BTK抑制剂耐药的6例患者中,ORR为50%,包括1例CLL和BTK C481S突变的患者。
迪哲凭借技术平台持续不断地产出穿透血脑屏障的小分子抑制剂,公司未来有望收获全新的BD交易。
结语:正因为研发穿透BBB的创新管线资产的门槛较高,可能决定了未来在这个领域投资者的选择并不多,这样带来的好处是押中收获重磅BD的公司概率将极大提升,显然这是一个合乎逻辑的投资思路,也是创新药投资者无法忽视的。











