3月12日,国家药监局发布通告,批准南京诺唯赞、北京金沃夫、深圳华大因源、广州万孚生物、北京华科泰生物的新冠抗原产品自测应用申请变更。自此五款新冠抗原自测产品正式上市。此前相关产品的可使用范围只有医疗机构端,由经过专业培训的人士使用;变更后,则可自行购买、居家自测。

来源:NMPA
3月11日,国家卫健委官网公布了《关于印发新冠病毒抗原检测应用方案(试行)的通知》,指出:国务院决定在核酸检测的基础上,增加抗原检测作为补充。此前体外诊断行业内已有相关消息传出,官方文件发布当日,IVD企业、四大药房等概念股纷纷大涨。
《通知》中明确了新冠抗原的三种应用场景,除基层医疗卫生机构抗原检测外,还包括隔离观察人员、社区居民的抗原检测,意味着“居家自检”将大范围用于新冠肺炎的筛查中。
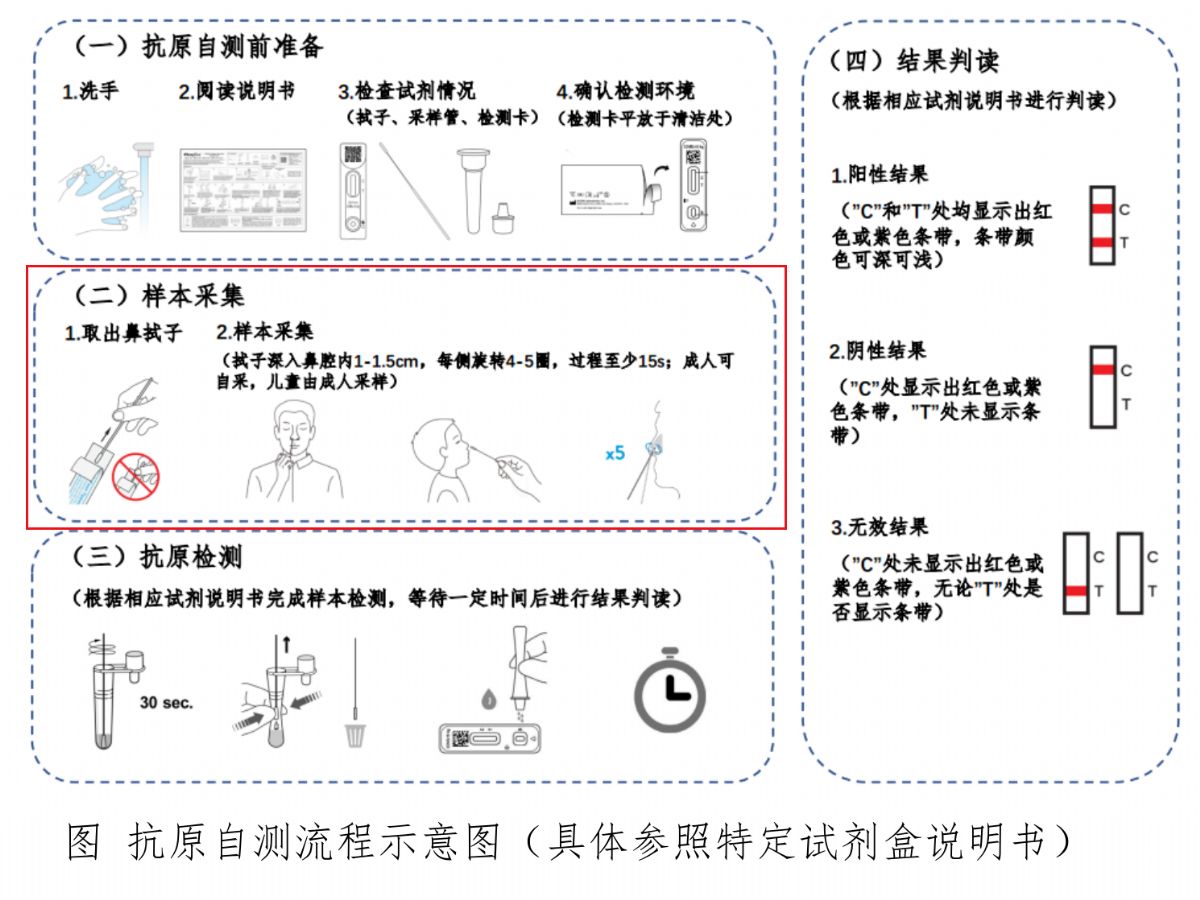
来源:《新冠病毒抗原自测基本要求及流程》
01、为什么要开放新冠抗原检测?
排大长队做核酸,是很多居民都体验过的检测场景。相比而言,抗原检测具备:出结果快(15-30分钟)、便宜、操作简单、无需专门仪器等优势。但因为抗原检测覆盖病程短,灵敏度低于核酸检测,低病毒载量的患者有可能被漏检(假阴性),所以核酸检测依然是金标准,抗原检测作为补充、用于初筛。
开放新冠抗原检测,是在核酸基础上,为人群快速、大规模筛查再加一道“早发现”的防线。从3月11日国务院联防联控组会议的要求来看,“落实从严从紧、精准防控、严而又严的要求,尽快阻断疫情传播途径,坚决避免疫情规模再扩大”,严防死守、避免反弹仍是当下工作要点。
11日晚,复旦大学附属华山医院感染科主任张文宏在接受媒体采访时表示,奥密克戎变异株使得新冠病毒传播速度加快,全国很多地区新增比较多的病例;此时完全依赖核酸,检测速度就会面临一定的挑战。因此,在采样不便、没有适当条件快速进行核酸检测时,可以选择简易的抗原检测。
“抗原的检测因为没有扩增,敏感性要稍微低一点,但一旦检测出阳性,就有很强的价值…..未来如果我们要面对更大规模的、国际开放以后形成的输入性病例,中国最终也会实现开放,过程中,我们始终要把病毒控制到非常低的传播水平,也就是说越早发现病毒,传播的人越少、隔离的速度越快,最终可以更快地实现社会面的清零。”张文宏教授在视频中表示。
从另一角度来看,核酸检测出结果往往需要6小时以上,存在高成本、耗时耗力、聚集风险等问题。当局部疫情爆发时,涉疫区域的多轮全民核酸检测是一笔不菲的财政投入;对个人而言,尽管核酸检测费用已降至35元/次,但对需经常因私出行者累积起来也是不少的额外支出。
从出厂价来看,抗原检测试剂盒的价格可降至5元左右,终端售价应不超过20元。根据《通知》来看,基层医疗服务机构的试剂纳入集中招标采购,通过省级集采,价格应与出厂价接近,甚至更低。如果用抗原检测替代相当一部分核酸检测,则有望降低财政投入和个人检测支出。
另外,对于医疗机构工作人员、口岸防疫和边防检查人员、冷链从业者等,每周一次核酸检测的频次,也要消耗相关人群大量时间。通过抗原检测作为早筛方式,能够大大减轻医护人员、医疗卫生机构负担。
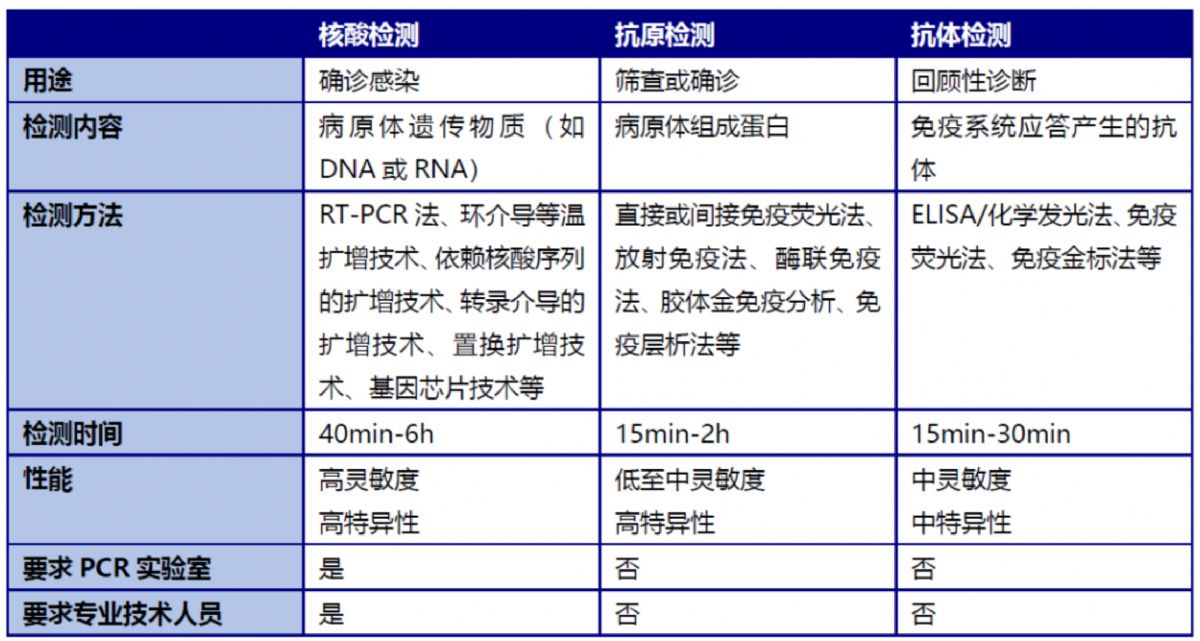
三种新冠病毒检测方法对比,来源:海尔施基因官网
其实,在全国性文件发布前,国内已经有部分重点区域/人群可选用抗原等快速检测方法。比如在海关闭环中,1月28日交通运输部等《关于做好国际航行船舶船员新冠疫情防控公告》中指出:“新冠病毒检测,应优先使用核酸检测,在不具备核酸检测的条件下,可选用抗原等其他快速检测方式。”
02、试剂盒如何才能获批?哪些企业获益?
目前,已经有5家企业新冠抗原产品在国内上市,分别是金沃夫生物、万孚生物、华大因源、华科泰、诺唯赞。变更后,原本只用于医疗机构端使用的试剂,被批准用于OTC家用自测。如今政策放开,上述企业将快速享有市场先发优势,被应用于基层医疗机构、隔离人员、以及居家检测的各类场景中。
新冠抗原自检在海外是重要的检测手段,已有数十家国内IVD企业在德国、美国等国家获批销售抗原检测试剂盒。其中,艾康生物、九安医疗、东方生物的抗原检测产品获FDA批准,可用于OTC居家检测。一位行业人士对36氪表示,针对居家场景的自测,企业对产品的研发和设计,应该力求简便快捷,减少人为因素对结果的干扰。

FDA批准新冠抗原EUA的OTC家用自测产品
在中国,新冠抗原检测试剂盒作为三类医疗器械,审批有着严格的程序,据国家药监局发布的《2019新型冠状病毒抗原/抗体检测试剂注册技术审评要点(试行)》:抗原试剂需在3家以上临床试验机构开展临床试验;灵敏度85%的情况下,“按照抽样精度公式估算确诊病例应不少于200例”,如特异度95%,排除病例建议不少于300例。
此前,业内就有观点认为:药监方面可能加速新冠抗原家用自检产品的审批;3月12日监管方连夜变更抗原检测产品生产批件,也显示出对此的支持态度。不过,国外已经上市、并规模化销售的国产抗原检测产品,在国内上市需如何开展临床试验,仍需等待监管方面进一步的细则。
对于已在海外获批、但尚未在中国拿证的企业,包括艾康生物、安旭生物、热景生物、万泰生物、唯实生物(菲鹏生物控股70%)、奥泰生物、博拓生物、明德生物、万孚生物、乐普生物、东方生物、亚辉龙、硕世生物、基蛋生物、艾康生物、九安医疗、东方生物等30余家企业,本土抗原检测政策的开放,于其而言,也意味着一大增量市场。
上述各家产品已研发完成,人员具备相关经验,且搭建了一定的产能,有能力快速响应政策。以艾康生物为例,作为首家获得FDA新冠抗原自检试剂EUA批准的中国企业,据FDA官方报道,艾康生物在2022年2月份实现一个月2亿份试剂的产能。经历过新冠疫情的考验,中国IVD企业在产能提升上已有充足的应对经验。
除产能外,对于IVD企业而言,销售渠道是另一个竞争要素。此前IVD试剂产品销售的主阵地是在医院,而对于新冠抗原试剂盒,一方面是面向基层医疗机构(集中招标采购),另一方面则是OTC市场,代理商资源、药房/医药电商等渠道也颇为重要。
其中,药房作为面向社区居民的重要渠道,也获得一定利好。3月11日四大药房(益丰、一心堂等)股价全部大幅上涨,侧面反映了市场对药房能借此实现业务增量的预期。
值得关注的是,新冠抗疫自测产品获批后,居民自行采样(鼻/咽拭子)实操的规范程度、数据追踪对接等仍需在试运行中跑通。
【免责声明】:本文不构成任何投资建议。市场有风险,投资需谨慎。
如有任何疑问,请联系(editor@zero2ipo.com.cn)投资界处理。












