9月9日,阿斯利康/第 一三共在2024 WCLC大会上公布了Trop2 ADC产品Dato-DXd(DS-1062a)治疗二线NSCLC的TROPION-Lung01三期研究OS获益结果,最终结果令投资者大失所望:在全体患者分析中,Dato-DXd组和多西他赛组的中位OS分别为12.9个月 Vs 11.8个月,HR为0.94,未达到统计学显著差异。
受到消息影响,第 一三共、阿斯利康的股价近日都有点绷不住了。
NSCLC不是个小适应症,即便是二线治疗也同样市场巨大。Dato-DXd是继DS-8201后,阿斯利康以60亿美元总包引进的ADC,如今在NSCLC遭遇挫折,让其前景蒙上不确定的同时,也给更多的Trop2 ADC竞争者让出了一条大路。
开启了数个NSCLC全球三期临床的科伦博泰SKB264,受益一马当先。
01
因失败而丢掉的市场
众所周知,非小细胞肺癌(NSCLC)占肺癌病例数近90%,几乎是全球肿瘤领域的新发/死亡的最 大细分适应症。其中,非小细胞肺癌又可以分为腺癌、鳞状细胞癌和大细胞癌,若按鳞状和非鳞状的方式区分,鳞状约占25%-30%,其余则是非鳞状病例。
鳞癌、非鳞癌各自具有不同的生物学和分子特征,并且鳞癌更加“难治”。鳞癌多位于中心位置,易于出血和坏死,此外还缺少EGFR等明确驱动基因,患者从VEGF抗血管生成药物、培美曲塞、靶向治疗中罕有获益或安全性不佳,多年药物开发进展缓慢。
Dato-DXd的TROPION-Lung01试验,共纳入604例患者,其中非鳞状NSCLC患者占比78%左右,伴有治疗驱动基因异常(AGA)大约17%左右,显然该试验侧重于验证Dato-DXd二线治疗局部晚期或转移性NSCLC患者的疗效与安全性。
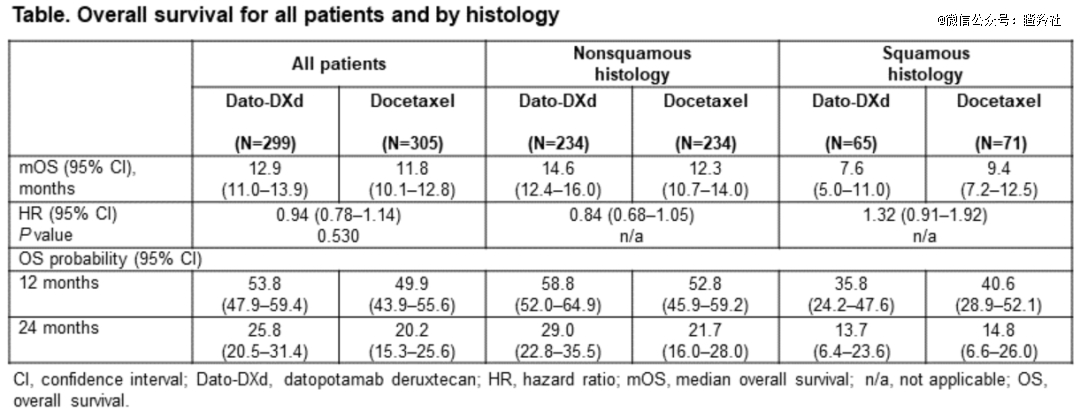
TROPION-Lung01研究中,Dato-DXd除了在鳞状NSCLC(简称:SQ)没有获益外,连在非鳞状NSCLC(简称:NSQ)患者中的效果也差强人意。
非鳞状亚组中,Dato-DXd组和多西他赛组的中位OS为14.6个月 Vs 12.3个月,HR为0.84,95%置信区间为0.68-1.05,不及预期的地方主要在于:其HR数据连续滑坡,低于ESMO 2023中期OS的HR 0.77和ELCC 2024的HR 0.79。
Dato-DXd在二线治疗的先发优势可能仅存在在于伴有AGA的NSQ患者中,
TROPION-Lung01研究数据显示,在AGA阳性的NSQ患者中,OS获益较为显著:15.6个月 Vs 9.8个月(HR为0.65,但置信区间上限为1.08)。
TROPION-Lung01研究OS分析的低于预期,直接导致了Dato-DXd丢失其在
NSCLC二线及后线治疗市场的核心竞争力。由此,杰富瑞调低了Dato-DXd获FDA批准的概率(80%→40%),此前其预计的Dato-DXd二线治疗NSCLC销售峰值为25亿美元。而悬在Dato-DXd头上的利剑还有TROPION-Lung01研究报告了7例患者因间质性肺炎(ILD)死亡,安全性风险也不容忽视。
为什么Dato-DXd在二线NSCLC中获批面临明显风险?一般来说,FDA要求置信区间上限低于1才能获得明确的批准路径,由于公司TROPION-Lung01研究完整分析的置信区间上限为1.05,所以FDA召开咨询委员会会议的可能性大增。
02
Trop2 ADC不止一次的失败
Dato-DXd不是唯 一一个在NSCLC后线治疗三期临床失败的Trop2 ADC。
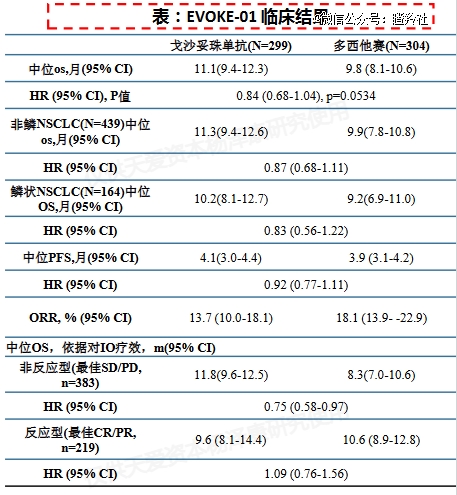
早在2024年初,吉利德的Trop2 ADC产品Trodelvy,同样在对比多西他赛治疗经治转移性或晚期NSCLC患者三期临床研究EVOKE-01未能达到临床OS主要终点。
从实验设计的维度看,EVOKE-01研究与TROPION-Lung01研究拥有一定相似性,前者入组患者为铂类化疗、免疫检验点治疗进展的二线NSCLC人群且不对Trop2表达做要求,后者入组患者要求则是既往至少接受过一线治疗的NSCLC患者,两个试验均旨在挑战“二线治疗NSCLC全人群”。
另外,两个研究入组人群的显著区别在于EVOKE-01没有入组伴有AGA的NSCLC病人,TROPION-Lung01入组患者至少还有17%伴有AGA,也正是这样的入组差异,伴有AGA患者亚组至少还给后者扳回了一城。
(图源:ASCO、建投医药)
不同的是,在EVOKE-01研究的亚组分析中,在对既往IO不响应(SD/PD)的患者中Trodelvy对OS的提升明显有利(11.8 个月 vs 8.3 个月,HR 0.75,0.58-0.97)。
EVOKE-01、TROPION-Lung01两大三期研究的折戟,给后来想冲“二线NSCLC全人群”的ADC敲响了警钟,它们至少说明不同NSCLC的病理类型对于药物响应情况具有很大差异,并且既往治疗的响应情况也会影响后线药物的响应情况。
两大研究的折戟是否意味着Trop2 ADC在后线NSCLC治疗的市场竞争力?不尽然。两大研究的折戟,很大程度是临床设计过于激进所导致的疗效不显著,我们在不同的亚组分析上仍能看到Trop2 ADC对部分患者的显著疗效;同时,Dato-DXd、Trodelvy毒副作用较大,未来更好的Trop2 ADC药物或有望突破现有药物的桎梏。
03
科伦博泰持续上
Dato-DXd的TROPION-Lung01研究折戟,对科伦博泰SKB264带来的获益未被充分计价。
科伦博泰的Trop2 ADC管线SKB264具备同类最 佳的潜力,尤其在二线NSCLC领域,已经初步展现出此种潜力。
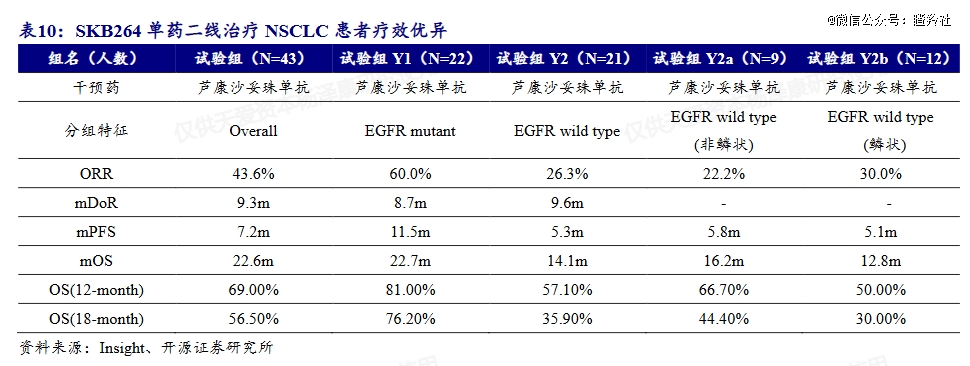
在II期篮式临床中,SKB264在全人群中ORR达到了43.6%,mPFS达到了7.2个月,患者总生存期达到了22.6个月;其中较为突出的亚组为EGFR突变的NSCLC患者群体,ORR高达60%、mPFS达到11.5个月和mOS达到22.7个月;虽然该试验样本量较小,但从Dato-DXd、Trodelvy全人群三期临床12.9个月、11.1个月的OS数据看,SKB264的疗效亦然非常显著。
安全性方面,SKB264安全性层面可控,3级及以上TRAE发生率69.8%,但未出现因不良反应导致的中止治疗或死亡;值得注意的是,SKB264目前为止并未在临床中发现有间质性肺炎相关的副作用。
在科伦博泰的努力下,SKB264即将进入商业化阶段,目前该药在国内已有两个适应症新药申请获得CDE受理,包括既往至少接受过2种系统治疗的局部晚期或转移性三阴性乳腺癌的NDA、EGFR-TKI和含铂化疗经治的局部晚期或转移性EGFR突变NSCLC,其中与本文相关的后者适应症已纳入CDE的优先审评审批程序。
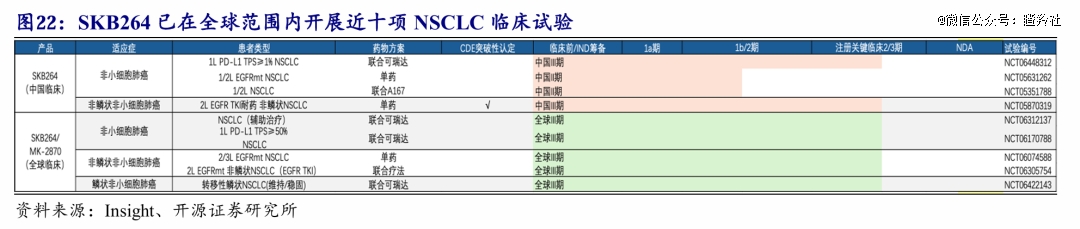
在合作伙伴默沙东的助推下,SKB264已经在全球开展5项三期临床。从各个MRCT的适应症上看,默沙东的临床策略稳扎稳打,在后线治疗领域选择了SKB264前期数据更为出色的EGFR突变NSCLC,一线治疗则是选择了PD-L1 TPS大于等于50%的人群。
在与K药联合治疗方案的层面,SKB264在2024 ASCO大会公布的二期数据显示:SKB264联用塔戈利单抗(PD-L1)一线治疗NSCLC患者的低剂量组mPFS超过了15.4个月,较贝伐珠单抗联合紫杉醇和卡铂一线标准治疗延长了9.2个月。
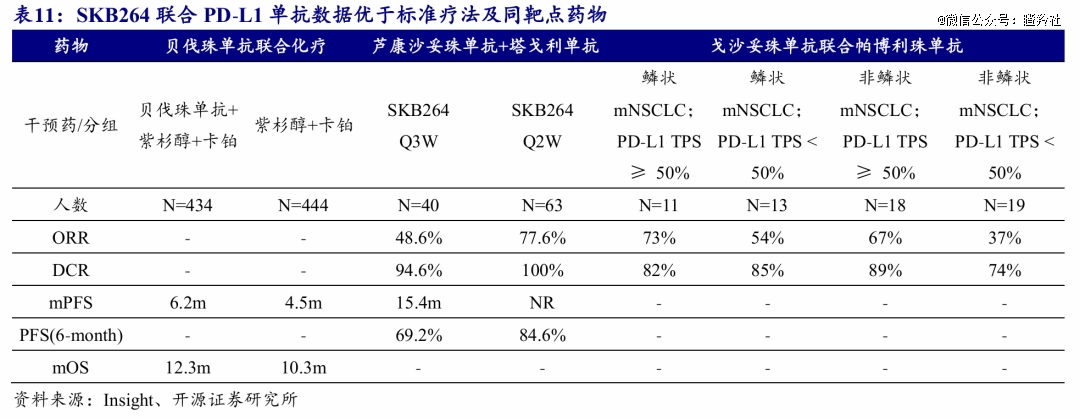
足以看出,SKB264不仅存在同类最 优Trop2 ADC的潜力,同时在默沙东和其K药的助攻下,其选择了一个最合理、最稳健的探索NSCLC适应症潜力的方式,这很可能将为其后续的大获成功埋下伏笔。
结语:最 强ADC“Dato-DXd”的城寨并不像媒体宣传的那样坚不可摧,后来的国产ADC分子可以通过差异化的适应症布局、安全性改良、聚焦前代ADC耐药后线治疗等方式去后发蚕食市场份额,再通过逐步进军前线,完成对这个巨人的对抗甚至超越。
有默沙东加持的科伦博泰和它的SKB264,潜力无限。
【免责声明】:本文不构成任何投资建议。市场有风险,投资需谨慎。
如有任何疑问,请联系(editor@zero2ipo.com.cn)投资界处理。












