一个发展了近百年的市场,这两年在中国却有了“翻红”的迹象。
2021年,国家八部门联合制定的一纸文件按下了行业加速键。这份中国*针对核技术在医疗卫生应用领域的纲领性文件——《医用同位素中长期发展规划(2021-2035年)》掀起了中国核药市场的骚动。而在今年9月和10月,两个政策的颁布给“核药热”再添了一把火。
短短两年间,已有数家企业如先通医药、辐联医药、药明博锐等企业先后获得巨额融资,开始抢滩。辐联医药更是在上半年刚完成A轮融资后,就斥资2.45亿美元大举收购。
核药由载体(即普通药物)和放射性核素组成。通俗而言,它就是将“核弹”装载在载体上然后送入指定位置,利用“核弹”产生的α、β或γ放射线将消灭或找出病变组织。
在中国,这个长期被双寡头霸占的市场,随着新鲜血液的不断涌入,如今有了松动的迹象。
要知道,从上世纪50年代*核药碘的出现,全球核药市场就已兴起。只是,中国的核药市场虽然也由此起步,但过去数年间都稍显沉寂。
一位业内人士曾不免感慨:“5年前或者10年前谈核药时,都很悲哀地说,我们所用的这么多核药没一个是在中国弄出来的。”
中国的核药市场为何会落后全球市场一拍?再度“翻红”的它又还能走多远?我们将在下文一一回答这些问题。
01 中国核药难产
中国核药市场的发展,是有些慢热的。
它的起步,大概可追溯至核药碘被FDA批准的那一年。那个时代,美苏争霸中常常显示核威慑力。约四五年后,中国出于国际格局的考量,也加紧迈入核研究。1956年,中国制定了12年科学远景发展规划,核药站上历史舞台——“同位素(核素)在医学中的应用”被列为国家重点科研项目。
同年,*同位素训练班诞生,中国研制出了*批放射性标记物并建立初步的医用放射性核素与药物生产线。
从上世纪80年代起,中国核医学迎来了快速发展。一方面,1989年国务院颁布《放射性药品管理办法》,对国内“核药”的生产环节进行规范化管理;另一方面,产品倍出——99mTc标记药盒、质子回旋加速器、18F核素相继出现,而随着SPECT及PET/CT等设备的国产生产商不断涌现,核医学市场在中国正式开启。
只可惜,这个火苗没能烧旺起来。过去数十年间,中国核药的创新研发近乎停滞,以致于近几年,中国没有一例创新型核药获批。
数据同样可以佐证这个残酷的现实。截至2020年7月,FDA共批准了52种核药,其中多种产品在中国并无企业获批。“过去根本没有这个技术力量。”中山大学附属*医院核医学科主任张祥松曾如此坦言。
02 为何难产?
对于中国核药而言,受限是全方位的。
除去研发实力与海外的差距,核药研发和生产的前提——核素,中国就难以规模化国产。目前,中国除少量碘-131和镥-177外,大部分核素如钼-99、碘-125、锶-89等都依赖于进口。
尽管在全球化的当下,核素需要进口不是什么根本问题,但由于核素的特殊性,以及海外核素供应商一般倾向于和现有客户保持合作而非建立新业务关系,对于新进入者而言,如何让供应商按合理价格稳定供给,就成了一大挑战。
到生产环节,问题再次出现。部分核素如PET /CT的配套影像剂18F-FDG 系列药品需要利用回旋加速器生产,这又是中国被“卡脖子”的一环。眼下,国内PET用回旋加速器市场主要被日本住友重机械和GE两家占据。
近些年,中国正高呼“国产替代”,但在核药生产环节,难度依旧颇高。一是核素的放射性,大型核反应堆或回旋加速器,其建造和运作都有较高的技术门槛和异常严格的规定。二是核药涉及复杂的放射性示踪技术及放射性检测技术。单就这两项就劝退了不少试图入场者。
再者,核的危险性,让核药的监管严格和复杂程度远超常规药物。单从涉及的部门数量来看,一家企业要想开发核药,就需要通过国家核安全局、公安部、卫健委、海关总署、交通运输部、中国民用航空局、国家国防科工局等多个监管部门的资质认证。
跑完这样一套流程费事费时不说,即便层层打通这些关卡,拿到药品批文要想迅速实现药品销售放量,也是难乎其难。品牌认知和物流配送,都是重大障碍。
核药壁垒高筑,是中国核药难产的原因,也是后来者难以逾越的护城河。
03 谁在二分天下,筑壁垒?
因此,在中国,这笔生意虽然价值超百亿美金,但很长的一段时间里并没有被过于市场化。国家相关核研究院的下属企业,是这个半开放市场的主要玩家。
依托中核集团的中国同辐,便是双寡头之一。作为中国核药的老大哥,中国同辐旗下核药产品品种最全。此外,它还是中国* 一家具备辐照用钴 [60Co]、医用钴[60Co]等生产能力的生产商。
而另一位寡头——以原料药起家的东诚药业,则是通过收购云克药业——前身是中国核动力研究设计院成都同位素应用研究所进入核药领域,云克注射液和碘[125I]密封籽源、锝[ 99mTc]替曲膦注射液等为其主要产品。
与海外市场相似,中国的核药市场同样是治疗和诊断市场二八分天下。而从竞争格局来看,中国同辐和东诚药业已经将国内核药市场份额几乎收割殆尽。从版图来看,它们通过核药房的布局,也在中国各自跑马圈定了势力范围。
通俗理解,核药房就是集生产、管理、配送和服务的核药中心。由于核药尤其是诊断用核药的半衰期较短,因此其生产、贮存和配送都对企业提出了较高要求。
目前,中国的核药房资源几乎都集中在这两家公司,各自约有20家左右。其中,东诚药业的核药房几乎是沿着中国黑河-腾冲人口分布线布局。
然而,就是如此二分天下的局面,“双子星”似乎也没想着给后来者留下机会,它们不断收购公司建造全产业链,不断建设核药房,从而继续垒高护城河。要知道,核药房的建设周期基本都要3年起,投资约3000至5000万元,因此,若不是有足够的财富积累,很难在核药房资源上竞争。
04 “双寡头”格局开始松动
但换个角度,这也是双寡头急需稳定江山之举。近年来海外核药市场的不断刺激以及国内政策和产业环境逐步完善,已经在培育新的挑战者,松动双寡头格局。
海外核药市场进入2012年后,陆续有核药获批,一些企业也开始寻求开拓中国市场。2014年,美国核药企业Navidea的新型受体靶向放射性药物Lymphoseek® ,一款99mTc标记的核药获FDA批准,随后该公司希望能开拓中国市场,开始在中国寻找合作伙伴。
彼时,还专注在仿制药业务的先通医药抓住了这个机遇,开始转型布局创新型核药。那是核药在中国还少有人问津的时代,也是东诚药业刚决定进入核药市场的时候。但美国核药市场的繁荣,让先通医药有了专注做创新核药的决心。2019年年底,先通医药彻底剥离了原来的传统药物。
站在今天来看,先通医药那时的选择的确踩住了风口。
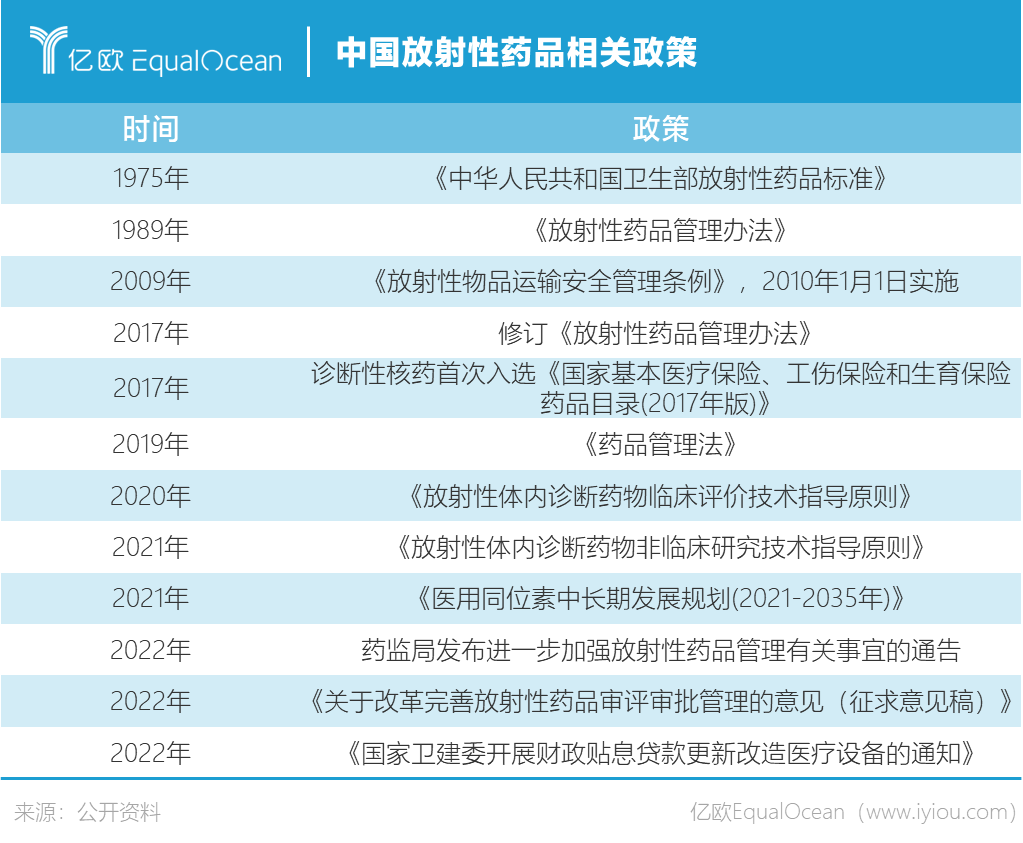
2021年5月,对于核药物行业来说是一个标志性节点。彼时,国家原子能机构联合科技部等八部委联合发布《医用同位素中长期发展规划(2021-2035年)》,这是中国*针对核技术在医疗卫生应用领域发布的纲领性文件。
文件指出到2025年,一批医用同位素发展的关键核心技术取得突破,适时启动建设1-2座医用同位素专用生产堆,实现常用医用同位素的稳定自主供应;到2035年,积极推动医用同位素“走出去”。
政策春风拂动,发展已有百年的核医学,在中国终于“翻红”并走上正轨,来到了爆发前期。文件颁发后,数家核医学企业斩获新一轮融资——智核生物完成亿元C轮融资,而刚在2月份完成3.2亿元D轮融资的先通医药,仅过了8个月,又被资本追加3.2亿元融资。
时间来到2022年9月和10月,国家药监局公开征求《关于改革完善放射性药品审评审批管理的意见》,中国同位素与辐射行业协会又出台了《核医学科建设规范(征求意见稿)》,政策的密集发布,开始推动核药产业链的发展。
也是在这一年,红杉中国接连领投两家核医学企业——辐联医药完成近2.5亿元A轮融资、药明博锐完成近3亿元A轮融资。同期,晶核生物也完成了近亿元天使轮融资。
从这些企业专注的细分领域来看,我们或许可窥探核药的下一个风口。其中,药明博锐所专注的新一代靶向核素偶联药物(RDC)领域,就被视为肿瘤靶向新星。在国内,这一赛道刚处于起步阶段,布局的企业并不多,除了药明博锐,远大医药算是是布局治疗及诊断性RDC药物最多的企业。
05 结语
近两年,随着中国核药市场火热,资本已经纷纷涌入该赛道。只是,在设备渗透率有所提升、政策逐步完善、资金更为充足的情况下,核药发展的另一个致命缺点也在逐渐暴露,那就是核药物研发人才资源稀缺。
实际上,核药属于多学科交叉领域,涉及药学、辐射剂量学、辐射生物学以及放射化学等多个专业,体系复杂,壁垒高。而像药明博锐这样由北大放射化学学科带头人刘志博带头,又获得药明康德加持的企业,并不多见。
专业人才难招,也成了短期内摆在国内核药企业面前的难题。不过,我们有理由相信,随着核药的前景在国内逐渐清晰,这些问题都终将迎刃而解。
【免责声明】:本文不构成任何投资建议。市场有风险,投资需谨慎。
如有任何疑问,请联系(editor@zero2ipo.com.cn)投资界处理。













