重庆发现内地首例猴痘确诊病例,近岸蛋白可提供猴痘抗原/抗体/分子诊断酶等原料
9月16日,重庆市卫生健康委员会对外发布消息称:重庆市确诊 1 例境外输入猴痘病例,猴痘病毒首次传至国内。
猴痘的历史
从1958年,科学家首次发现于一组用于研究的猴子体内出现“痘状”传染病,到1970年,刚果一名9个月的男婴感染猴痘病毒,成为全球首例人类感染猴痘病毒的病例,猴痘是一种人畜共患病的传染性疾病,症状类似于天花,包括发烧、肌肉疼痛和水疱。虽然天花病毒在1980年已在世界范围内被根除,但猴痘病毒仍然在撒哈拉以南非洲中流行 。猴痘一直未被国内重视,而这一状态在今日被打破,9月16日,重庆市卫生健康委员会对外发布消息称:重庆市确诊 1 例境外输入猴痘病例。经过检测,该病例感染的猴痘病毒属于西非系B.1支。
截至2022年9月19日,全球已经有104个国家/地区确诊,共61,406例病例,其中美国确诊最多,已有猴痘病例2.3万,死亡1例,中国内地出现首例。
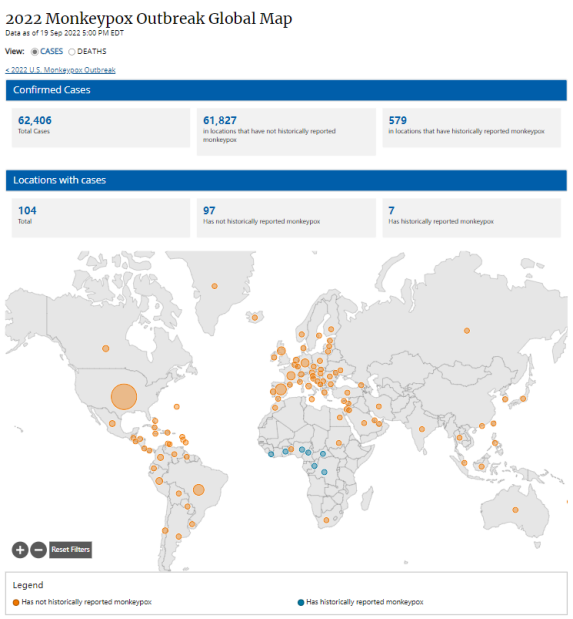
来源于:CDC官网
猴痘的特点有哪些?
01、耐干燥和低温,在土壤、痂皮和衣被上可生存数月。02、对热敏感,加热至56℃ 30分钟或60℃ 10分钟可灭活。03、紫外线和一般消毒剂可灭活。04、对氯仿、次氯酸钠、氯二甲酚、戊二醛、甲醛和多聚甲醛等敏感。05、基本传染数R0值<1(新冠肺炎R0值高达5.7),表明其传染力较弱。
猴痘是怎样感染发病的?
猴痘由猴痘病毒引起,猴痘病毒(Monkeypox virus,MPV)属于正痘病毒属(Orthopoxvirus genus),是一种有包膜的双链DNA病毒(≈197 kb),形态为卵形或者砖形,大小为200×250 nm[4]。猴痘病毒有两个不同的基因分支,即中非(刚果盆地)分支和西非分支。刚果盆地分支历来引起更严重的疾病,并认为更具传染性。到目前为止,这两个分支的地理区域界线一直在喀麦隆,这是*同时存在两种病毒分支的国家。
猴痘病毒在自然界主要存在于非洲的啮齿类动物(非洲松鼠、树松鼠、冈比亚袋鼠、睡鼠等)体内。灵长类动物(猴、黑猩猩、人等)接触感染猴痘病毒的啮齿类动物后也会感染。感染了猴痘病毒的动物和猴痘病人都是这个疾病的传染源。猴痘病毒的主要传播方式是通过直接接触到受感染的动物的血液、体液、皮肤或粘膜伤口。猴痘病毒主要经黏膜和破损皮肤侵入人体。人主要通过接触感染动物的呼吸道分泌物、病变渗出物、血液、其它体液,或被感染动物咬伤、抓伤而感染。人与人之间主要通过密切接触传播,也可在长时间近距离接触时通过飞沫传播,接触病毒污染的物品也有可能感染。本次猴痘疫情还发现多数病例在发病前有同性性行为,可能主要还是与性活动中的密切接触传播有关,目前尚不能确定是否会经过精液或阴道分泌物传播。猴痘病毒还可通过胎盘从孕妇传播给胎儿[5]。猴痘的潜伏期为5至21天。疾病的发热阶段通常持续1至3天,症状包括发烧、剧烈头痛、淋巴结肿胀、背痛、肌肉疼痛和剧烈虚弱。发热阶段之后是皮疹阶段,持续2至4周。病变从斑疹(基部平坦的病变)发展为丘疹(凸起的坚硬疼痛性病变),再到水疱(充满透明液体)再到脓疱(充满脓液),然后是结痂。在有记录的病例中,死亡患者的比例在0 -11%之间变化,并且在幼儿中更高。
猴痘病毒示意图(来源于WHO官网)
猴痘的预防和治疗
美国食品和药物监督管理局(FDA)许可两种疫苗可用于预防猴痘感,JYNNEOS(也被称为Imvamune或Imvanex)和ACAM2000。JYNNEOS是一种在人体细胞中无法有效复制的活病毒疫苗,ACAM2000是一种具有复制能力的牛痘病毒活疫苗。ACAM2000比JYNNEOS具有更大的某些严重副作用风险,不能提供给免疫功能低下或患有心脏病的人。
国内猴痘的防控政策
目前,国内尚无抗猴痘病毒药物。治疗主要包括对症支持治疗和继发性细菌感染的治疗。我国针对猴痘的防控工作主要集中在应对猴痘疫情输入风险。2022年8月10日,国务院联防联控机制举行新闻发布会,将继续加强对猴痘的防控工作,做好猴痘诊断试剂、治疗药物和疫苗的准备,实现早发现、早报告、早隔离、早治疗。2022年6月,国家卫健委发布猴痘防控技术指南(2022年版)的通知,其中规定现有入境人员隔离期间,在排查新冠病毒感染的同时,各地应主动对入境人员进行猴痘病毒排查,特别是入境前21天内有猴痘疫情报告国旅居史的人员;中国疾控中心也发布了《猴痘防控技术指南(2022年版)》,对各地做好猴痘的诊疗防控工作提供了指引。国外猴痘疫情更不容乐观,在2022年7月23日,世界卫生组织就宣布猴痘疫情为“国际关注的突发公共卫生事件”,这是WHO可以发布的*别公共卫生警报。
面对猴痘病毒在非流行国家和地区爆发,能够对猴痘病毒进行精准诊断以及特异性预防/治疗成为迫切需求。
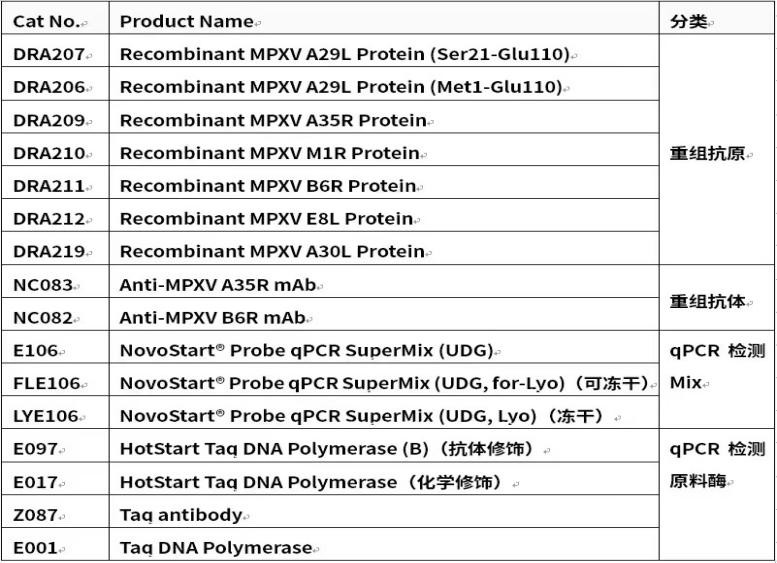
近岸蛋白提供重组猴痘病毒抗体/抗原,以及分子诊断酶,可用于疾病诊断、疫苗和药物开发。此外,以其应用技术开发平台为基础,还可提供重组亚单位疫苗、mRNA疫苗等CRO服务,加速下游客户研究进程。
相关资讯
- 自主创新引领未来!森普瑞斯生物信息转化创新平台亮相第二十八届科博会
- 客流变订单,订单变增长|PhotonPay光子易赋能外贸企业全球经营
- 深圳出海中心正式启动 政策护航、科技赋能,助力企业高质量出海
- 中国家电网成立清洁电器“反虚假测评联盟” 京东与25家品牌率先加入
- 燃情五一,炽热盛夏!SNH48的五月,每一步都踏在追梦的节拍上
- 脑机接口开启“数字桥梁”新局,微美全息(WIMI.US)多路创新探索并进风头正劲!
- PhotonPay光子易荣获万事达卡三项大奖,持续深化全球支付能力布局
- 小鹅通 Claw 正式发布 助力商家实现私域全场景高效经营
- 品牌全球化智能营销服务商博鼎国际完成数百万美元Pre-A轮融资
- 雅阁酒店集团|海景影音房惊喜上线,享受专属“私人影院”
- 尼尔森IQ BASES推出BASES人工智能产品测评工具,开创新方法