近期,一则高达1亿美金的种子轮融资消息在行业里被刷屏,成为截至目前,今年医疗领域*一笔种子轮融资。
众所周知,在创投行业,种子轮是创业公司获得的*笔重要资金,由于此时项目十分初创,平均融资额往往在数十万至数百万美金之间,鲜有企业能拿到数千万,甚至上亿美金。
“如果一家刚运营的项目能拿到上亿的大额融资,一般都是背后的创业团队极其牛,且项目发力的方向是大热门,二者往往缺一不可。”行业投资人龚莫告诉动脉网。
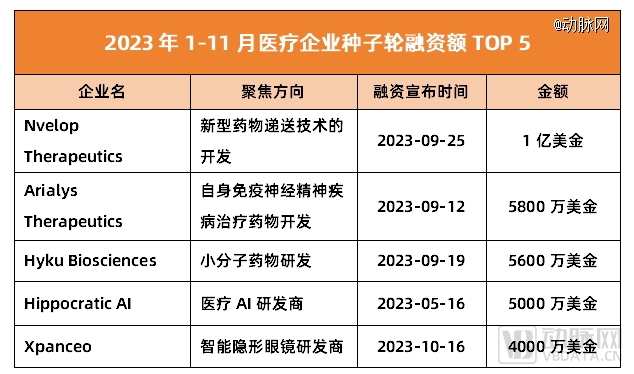
数据来源:动脉橙数据库
此次拿下1亿美金种子轮的企业名为Nvelop Therapeutics,成立时间仅1年。该企业背后的创始人为哈佛大学教授、基因编辑先驱刘如谦(David Liu):其除了是学术大牛外,亦拥有丰富的创业经验,主导或参与了Prime Medicine、Editas Medicine、Chroma Medicine、Exo Therapeutics等多家知名企业的创办。其中,Prime Medicine、Editas Medicine等已成功IPO。
而在业务方向上,Nvelop Therapeutics主要聚焦于新型递送技术的开发,这一领域目前正是医疗行业的大热门。根据动脉橙数据库显示,这一年多以来,药物递送赛道共有超10起融资事件,总融资金额逾30亿元。背后资方包括高瓴创投、MPM Capita、磐霖资本、泰煜投资、夏尔巴投资、险峰旗云、源码资本等一众知名机构。
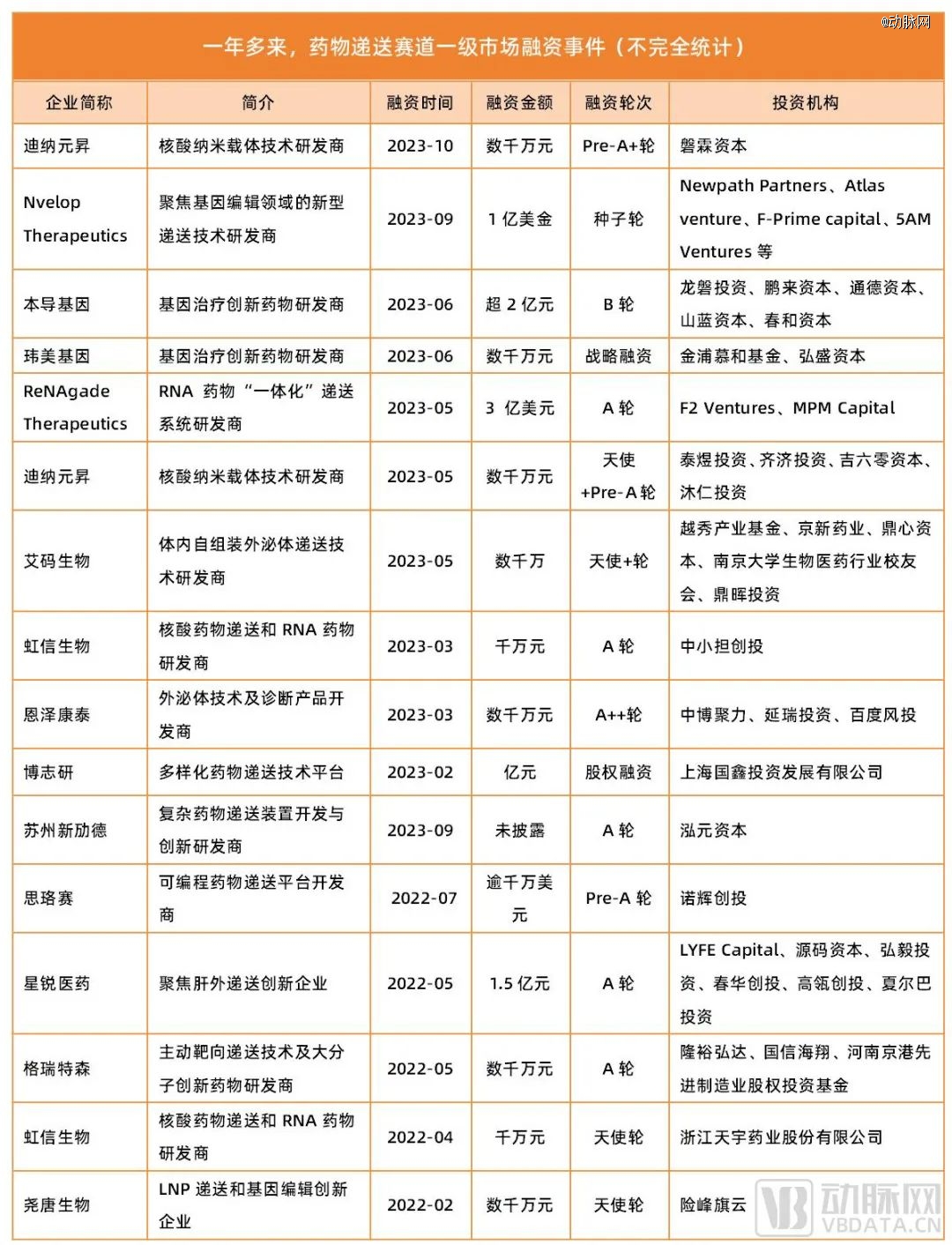
数据来源:动脉橙数据库
频获融资背后,药物递送赛道正在讲述怎样的新故事?
1、拿下今年*医疗种子轮融资,Nvelop Therapeutics凭什么?
在医药研发领域,药物递送被行业普遍认为是新一代技术的主力战场。
“药物递送在临床中极其重要。一是因为它会影响药物最终发挥药效的作用大小,二是决定了药物研发成败的关键点。”行业投资人龚莫告诉动脉网,药物递送系统往往承载着“药物靶向”、“药物控释”、“促进药物吸收”、“增强药物属性”四大核心功能,在产业链中价值巨大。
正是基于此,药物递送受到了行业的广泛关注。而身处这一热门赛道,加之创始人的丰富背景,Nvelop Therapeutics一诞生便具有明星光环:该企业以期通过切入递送技术领域,来释放基因治疗的更大潜力。
要知道,在基因编辑领域,由于细胞膜的特殊性质和治疗性基因材料的复杂性,基因编辑药物在人体内并不稳定,所以一旦药物靶向错误靶标,很容易对人造成严重的副作用。因此,如何将基因编辑药物递送至合适的位置,一直是行业最为关心的问题之一。
在这一方向上,Nvelop Therapeutics的创始人刘如谦进行了多年研究,其于2022年1月与合作者在《Cell》期刊上发表了论文《Engineered virus-like particles for efficient in vivo delivery of therapeutic proteins》。论文提到,目前在临床应用上,主要有病毒载体(慢病毒、AAV等)和非病毒载体(LNP等)两种,但这些载体尚有诸多不足,以AAV为例,其就具有装载能力有限(仅为5KB的DNA)的缺点。
针对此,刘如谦与团队开发出一种工程化类病毒颗粒(eVLP),其能够高效地将基因编辑工具递送到动物体内的细胞中。eVLP具有不少亮点,比如论文表示,eVLP递送的碱基编辑对小鼠肝脏63%的细胞进行了有效编辑,成功将血清中PCSK9水平降低了78%。
此外,研究团队在对eVLP递送的体外和体内基因编辑的DNA水平和RNA水平脱靶情况进行检测后发现,无论是DNA还是RNA,都未检测到脱靶,而这与AAV病毒或质粒载体递送相比,优势明显。
Nvelop Therapeutics正是以上述研究为基础而成立的公司,而1亿美金的投资,足以表明投资机构们对eVLP应用潜力的认可。
在团队组成方面,除了刘如谦外,哈佛大学教授J. Keith Joung担任联合创始人,后者亦是基因编辑公司Editas Medicine、Beam Therapeutic、Pairwise Plants的联合创始人。其中,担任CTO的是Jeffrey Hrkach博士,其曾在生物制药公司Moderna和Frequency负责递送研究。可见,明星管理团队的加持是Nvelop Therapeutics能够迅速起势的原因所在。
据LinkedIn显示,Nvelop Therapeutics正在持续扩招,目前已招募数十位员工,他们主要来自疫苗、细胞疗法和基因治疗等多个细分领域,团队具有多学科交叉的复合产业背景。
综上,正是身处药物递送赛道、拥有前沿的递送解决方案与明星创始团队阵容三大要素的汇集,使得Nvelop Therapeutics在成立仅一年多时间里,便拿下1亿美金大额种子轮融资。
2、掀起资本热潮,药物递送赛道进展几何?
在一年多时间里,投资机构们砸下超30亿元的资金,开启了新一轮药物递送赛道融资热潮。
“无论是基因治疗,还是小分子药、大分子药,其实都离不开递送技术。”行业投资人龚莫表示,从体外微针注射递送小分子化学药剂,再到用脂质体(LNP)包裹大分子药物体内递送,递送系统可谓无处不在。
但同时,药物递送赛道投资并不容易。“投资药物递送赛道需要理清一系列关键问题。每种载体技术都各有特点,那理想的递送载体究竟需要具备哪些属性?如何辨别各自的商业化前景?”在龚莫看来,药物递送系统要观察两个基本面,一是在技术与临床角度,装载能力、靶向迁移能力与安全性是否优秀,二是在生产制备角度,是否可以规模化发展。
因此,把握好技术流向与商业价值判定具有重要意义。
在技术流向上,笼统地来说,药物递送系统可以分为体外递送和体内递送两大类。其中,体外递送包括微针、贴片等。目前,一级市场相对关注更多的是体内递送。
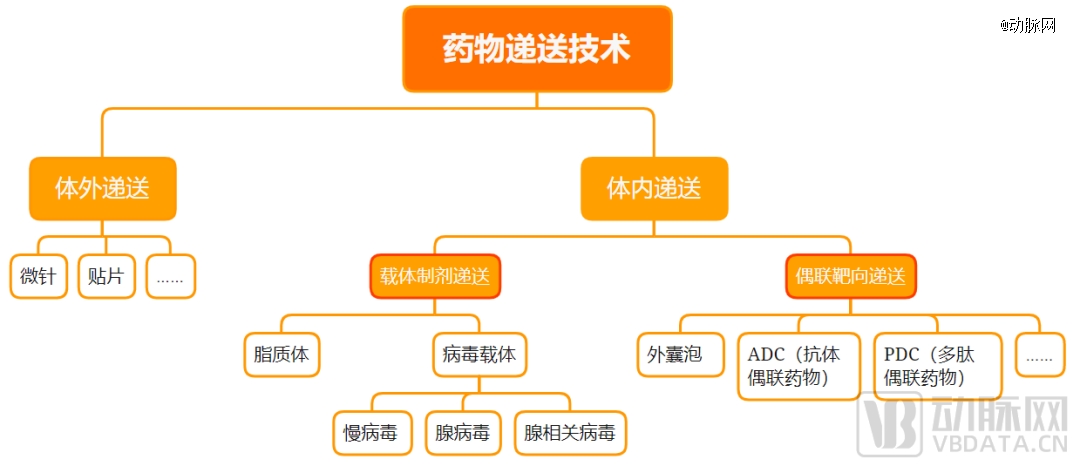
药物递送技术分类 动脉网制图
将体内递送再往下拆分,主要可归纳为载体制剂递送、偶联靶向递送两个方向:载体制剂递送是指需要通过独立载体进行包装后进行的药物递送,偶联靶向递送则是将靶向分子与药物分子通过化学键偶联起来形成创新药。
“不同的递送技术,往往有与之最契合的药物。”行业投资人龚莫表示,对技术的运用要与临床场景相挂钩。
正是基于此,体内递送领域正“百花齐放”,新旧载体都有其发挥作用的舞台空间。
具体来看,载体制剂递送这一方向目前有脂质体(LNP)、病毒载体、外囊泡(EVs)等主流递送载体。
作为通用的纳米载体平台,脂质体可以运输疏水或亲水分子,包括小分子、蛋白质和核酸。目前,脂质体制剂已被批准用作药物和疫苗提供抗癌、抗炎、抗生素、抗真菌、麻醉剂以及其他药物和基因疗法。
除此之外,近年来脂质体(LNP)在mRNA疫苗递送上也受到了更多重视。原因在于,脂质体是球形囊泡,其可将mRNA包裹在内,从而抵御核酸酶的作用,以及脂质体类似于细胞膜,易与受体细胞融合,所以转染效率高。
以今年3月完成A轮融资的企业虹信生物为例,其就在脂质纳米粒(LNP)递送领域深耕,现已申请数十项发明专利,包括多项PCT和欧美发明专利,且已拥有完全自主知识产权的可离子化氨基脂质库。针对核心的可离子化氨基脂质,虹信生物完成了全球的专利布局,这为其mRNA创新药物管线开发以及对外授权合作开发奠定了基础。
又比如今年5月获得3亿美元A轮融资的ReNAgade Therapeutics。该企业在其全RNA系统中结合了包括新型脂质纳米颗粒(LNP)在内的递送技术,以期将RNA药物递送到以前无法进入的体内组织和细胞,从而消除RNA疗法的主要局限性。据STAT报道,ReNAgade Therapeutics的管线已完成体外与小鼠实验,并在进行多项非人灵长类的临床前实验。
病毒载体是最早被开发的生物药递送技术之一,并在细胞和基因治疗产业快速兴起的当下被人们所热议。
时下,慢病毒(LV)、腺病毒(ADV)和腺相关病毒(AAV)三个领域最受关注。其中,慢病毒(LV)是应用最为成熟的病毒载体类型,特别是在免疫细胞治疗(如CAR-T疗法)上起到了关键作用;而腺病毒(ADV)主要应用在疫苗领域;腺相关病毒(AAV)被更多应用于临床上的体内外基因治疗。
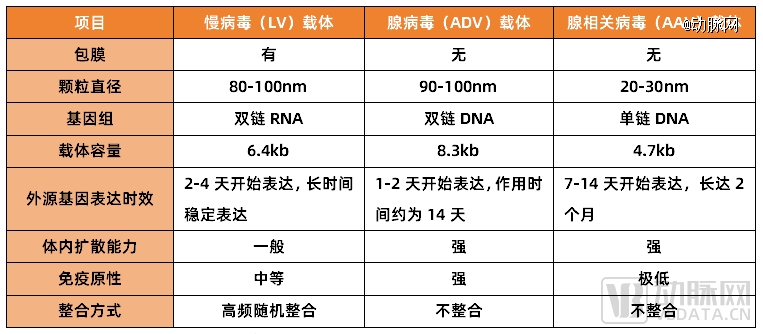
三种常用病毒载体特点对比 动脉网制图
目前,国内已经有不少企业在病毒载体方向布局,各个板块发展迅速,比如慢病毒(LV)的研发设计、加工生产就形成了比较明确的SOP(标准作业程序)体系,并向外延伸,促成了细胞治疗CDMO产业的快速兴起,机会十分广阔。
在这一方向上,已有多家企业拿下融资。比如今年6月完成超2亿元B轮融资的本导基因就搭建了自己的下一代慢病毒载体平台(BDlenti)。围绕着核心递送技术平台,本导基因布局了多条first-in-class的产品管线,开展了多项first-in-human临床研究,并与国际著名药企开展了重大神经系统疾病新型疗法的合作研发。
同月获得数千万元融资的玮美基因则建立了全面的腺相关病毒 AAV 改造平台——AAVMeta。据悉,该企业*眼科新型 AAV载体已成功实现商业转化,并借助载体开发的药物已进入临床实验阶段。与此同时,玮美基因还成功开发了用于耳蜗、肺部、神经系统和肌肉等多种不同组线的新型 AAV 载体,并在国内外的基因治疗疾病领域展开了广泛的专利布局。
外囊泡(EVs)为天然的生物大分子载体,其能像投递包裹一样将生物大分子从一个细胞传递到另一个细胞里面,进而实现细胞间沟通。
作为药物递送载体,外囊泡(EVs)具有不错优势,包括多重载药能力、良好的组织和血脑屏障透过性、表面容易装饰等。而根据不同的大小、合成方式、生物学性质,外囊泡(EVs)又分为多种不同的亚型,例如外泌体、微粒/微囊泡、肿瘤小泡、凋亡小体等。
比如今年3月拿下数千万元A++轮融资的恩泽康泰,该企业基于其旗下核心知识产权的工程化外泌体平台Echosome®来帮助外泌体创新药研发,现已建成3000平米外泌体GMP中试车间,并且建立成熟的外泌体生产工艺和质量表征体系,可提供工程化外泌体载体设计开发和工程化外泌体的CDMO服务等。
又比如2022年7月完成逾千万美元Pre-A轮融资的思珞赛,其对外泌体载药技术进行了创新性研发,独立开发了程序化药物递送系统(Programmable Drug Delivery)——TAXYTM。此外,该企业还开发了外泌体药物装载系统ExoPack,能将蛋白或核酸药物高效且具有选择性地装载到外泌体的内部或者表面。
再看偶联靶向递送。从偶联技术的维度来说,主要有随机偶联和定点偶联两种类型,二者都是用一个Linker(连接子)将药物和具备靶向递送功能的分子相连接,形成具有靶向递送功能的偶联药物。只是相对来说,定点偶联技术获得的产物均一性高,以及可降低杂质带来的毒性和不稳定性。
在这一方向,常见的有ADC(抗体偶联药物)、PDC(多肽偶联药物),其他主要为ABC(抗体生物聚合物偶联物)、ACC(抗体细胞偶联药物)、AOC(抗体寡核苷酸偶联物)、FDC(抗体片段偶联药物)、ISAC(抗体免疫刺激偶联物)、VDC(病毒样药物偶联物)等偶联药物。
其中,ADC当下受到的关注最多。就在10月20日-24日于西班牙马德里举行的“2023年欧洲肿瘤内科学会(ESMO)”上,ADC成为行业热议话题。20日当天,知名药企默沙东与*三共就三种ADC达成40亿美元合作,默沙东为其中的一款药物——R-DXd预付了7.5亿美元。未来,默沙东预计还将支付165亿美元的商业化里程碑款项,合作总额或高达220亿美元。这足以体现偶联靶向递送方向具有不错的商业合作空间。
不难发现,无论选择哪一个药物递送路径,核心是要能推动药物成功用于疾病治疗,并提高药物临床疗效和降低药物毒性等。这样的药物递送系统才是有价值,且被投资者所认可的。
3、 向未来进发,行业的挑战与新可能
自现代医药研发发轫以来,药物递送系统的研究便是贯穿其中且始终不变的热点话题。特别是在近年,随着生物药崛起,行业对药物递送技术的需求也越来越多。
在此背景下,多位投资人告诉动脉网,受益于基因疗法、RNA疗法等新技术的快速发展,药物递送载体的潜在市场被持续看好。而这,也将带动行业参与者在一级市场成为瞩目的焦点,以及在二级市场讲出更为性感的故事。
“载体本身不一定只是一种递送工具,它也有可能成为或诞生一种创新的疗法。这也是载体平台的魅力所在。此外,载体技术除了本身是新疗法的枢纽技术外,更重要的是其商业模式的灵活性。我们投资的公司将不再是把所有希望都赌注在单一靶点的成功与否,而是可以开创多种、多面向的合作,快速且不断地将不同疾病领域的疗法推进临床。”比邻星创投合伙人宋豪麟此前告诉动脉网。
大发展的背后,行业依然存在着不少挑战。比如外泌体的纯化就颇为复杂,加之哺乳动物细胞释放的外泌体数量相对较低,所以要如何获得高产量的纯外泌体,是入局者们要攻克的重点问题。
又比如腺相关病毒(AAV)的研发外包产业正处于起步期,行业内尚未有明确的共识,因此如何完善腺相关病毒(AAV)载体的GMP生产,仍是众多基因治疗企业需关注的关键要素。
当然,挑战即是机遇,当行业参与者们解决了一个又一个挑战,未来更多且更为高效、*的递送系统必会应运而生,从而助推生物医药的高质量发展。
在行业的潮起之中,中国药物递送领域的领军企业也势必会在接下来的一段时间里成批涌现。