要想成为Bigpharma,重磅炸弹药物必不可少。
吉利德便是得益于其“吉系列”丙肝治疗药物的成功,最终实现了市值上的飞跃:
2012年初,公司市值不过207亿美元;2015年,一度飙升超千亿美金,成为华尔街炙手可热的医药公司。
虽然因为疗效太好,丙肝神药“吉系列”随着患者人数的缩减而没落,但肝病领域依然值得关注。
在丙肝之外,乙肝也亟需医学界攻克,这是比丙肝更为庞大的市场。
也正因此,不仅是吉利德、罗氏、强生、葛兰素史克等海外巨头,国内东阳光药、腾盛博药、恒瑞医药、百济神州等纷纷参与其中。
目前,已经有一些药物,在临床阶段展示出功能性治愈乙肝的潜力。这或许意味着,“下一个吉利德”快要诞生了。
01、暂不能治愈的乙肝,未来的七百亿市场
乙肝的疾病危害无需多言。作为一种由乙肝病毒感染引起的肝脏疾病,乙肝在全球影响了将近3亿人的生活,国内便高达8600万。
目前的乙肝药物都需要长期服用。按理来说,我国乙肝药物市场规模有着极大的发展潜力。但与此相反的却是,我国乙肝药物市场规模正在逐年萎缩。
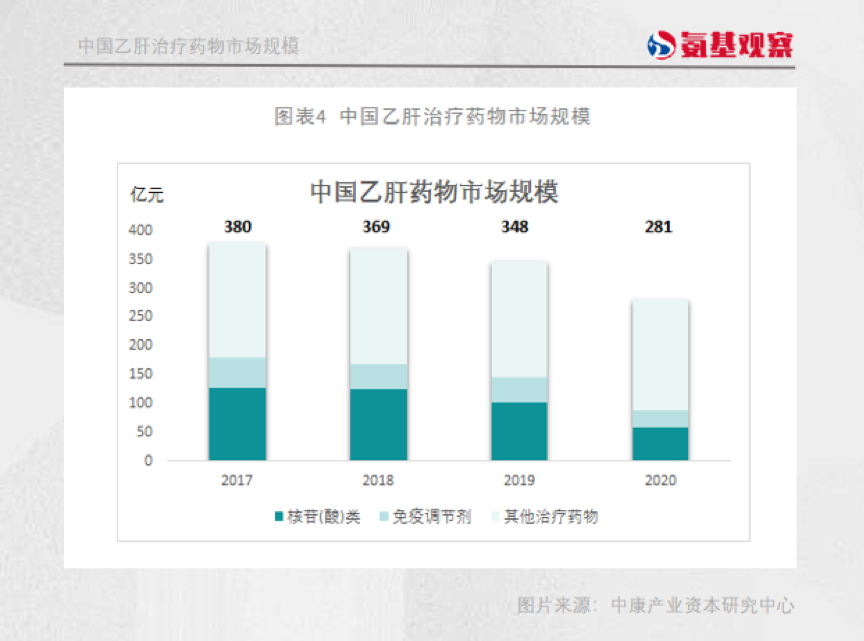
如上图所示,根据中康CMH数据,2017-2020年,我国抗乙肝药物市场规模分别为380、369、348与281亿元。这又是为什么呢?
背后原因在于两点,一是国内乙肝药物竞争逐渐加剧。
现阶段针对慢性乙肝的药物主要有两种,一种是干扰素另一种是核苷酸类似物。
不过,这两大类药品中的许多药物已经到了专利期,众多仿制药纷纷涌入市场,在集采的压力下,药价不断降低。
就拿阿德福韦酯片为例,在2021年已经有23家仿制药上市。压力之下,原研药企葛兰素史克直接在国内停产该药。
二是,我国乙肝患者的治疗率较低。
不管是干扰素还是核苷酸类似物,都有着自己的缺点。前者副作用较大需要注射使用,后者需要长期服药。当然最重要的缺点是,二者都无法实现乙肝的功能性治愈。
这也就导致了,患者的依从性较差,不愿意长期服药。叠加集采药物不断降价,乙肝药物市场不升反降也就不难理解了。
所以对于大部分创新药企来说,都没有选择在这两款老药上做无意义的内卷。而是选择研发创新型乙肝药物,将乙肝的功能性治愈作为目标。
在不少研发人员看来,虽然彻底治愈乙肝目前无望。但是功能性治愈乙肝,即HBsAg和HBVDNA持续检测不到、HBeAg阴转、伴或不伴HBsAg血清学转换,这个小目标还是可以冲一冲的。
据普华有策数据,随着更多创新型乙型肝炎病毒药物上市,仅中国乙肝市场将从2025年的156.9亿元增长到2030年的723.3亿元。
这仅是国内市场。实际上,全球范围内都未有乙肝治愈药物上市,因此市场注定极为可观。也难怪,全球主流药企,都在乙肝治愈方面开展攻坚战。
02、条条大路通罗马,全球药企竞速赛
目前围绕着乙肝的功能性治愈,主要有两条研发路径可走。
一条是直接抗病毒药物,直接靶向HBV抑制其复制,另一条是间接抗病毒药物,通过重新激活人体免疫系统来攻击HBV。
先来说间接的这条路,这条研发思路实际和急性乙肝自愈的过程大同小异。通过治疗性疫苗、免疫检查点抑制剂等来恢复免疫系统的杀伤力。
正在研发的TLR-7/8激动剂、PD-L1抑制剂、单克隆抗体都属于这条路。歌礼制药便在研发使用PD-L1对抗乙肝,腾盛博药则布局了单抗。
再来说直接的这条路。理论上来说,只要围绕HBV病毒生命周期的中的任一环节进行阻断,都可能显现出治疗乙肝的潜力。
顺着这个思路,多种针对HBV的药物进入临床研究。目前处于研发阶段的药物策略几乎针对HBV生命周期的每个阶段。
比如,病毒进入抑制剂。HBV与肝细胞受体的结合是HBV感染的*步,通过阻断二者的结合抑制HBV感染看上去行得通。
不过在实际临床中,病毒进入抑制剂对乙肝效果平平。比如,Hepcludex虽然对丁肝效果出色并成为了*获批治疗丁肝的药物,但对于乙肝并没能展现出降低HBsAg的潜力。
比病毒抑制剂更火热的,是HBV衣壳抑制剂的研究。
HBV入侵人体和大多数DNA病毒并无二致,不外乎吸附、侵入、脱壳、生物合成、组装和释放这一套流程。
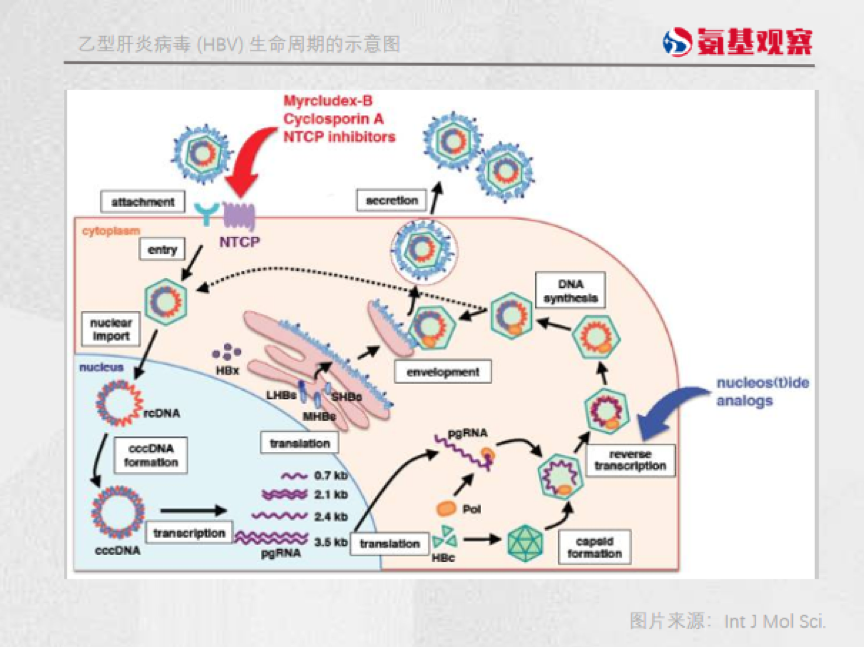
不过关键点在于,HBV与肝细胞受体结合后,双链松弛环状DNA(rcDNA)会进入细胞核,并利用人体内的材料将rcDNA加工为共价闭环双链DNA(cccDNA)。显然,cccDNA就是HBV入侵人体的*武器了。
而抑制衣壳分解的作用,便是阻止cccDNA的生成。因此,衣壳抑制剂成为了抗HBV药物的新靶点。
国外罗氏、Assembly,国内齐鲁制药、东阳光药、恒瑞医药、科伦医药等多家药企都围绕着这一路径研发乙肝药物。
不过,看起来仅凭HBV衣壳抑制剂单药抑制剂似乎很难实现乙肝的治愈。一项研究表明在体外抑制cccDNA的形成过程中,防止衣壳分解的机制可能是次要的。
使用NVR3-778、JNJ6379、RO7049389或ABI-HO731等衣壳抑制剂进行28天的给药临床数据也显示,衣壳抑制剂虽然对HBVDNA的对数减少有明显影响,但对HBsAg没有影响。
目前,不少药企在尝试研发更强效的衣壳抑制剂,及与其他疗法的联合应用以达到更强的治疗乙肝效果。
此外,针对HBsAg分泌抑制剂的研发也陷入了迷茫。因为目前针对HBsAg对于治愈HBV的作用,学术界也尚无定论。
看上去,想要实现乙肝的功能性治愈,仍然困难重重。不过,小核酸药的火热,为乙肝药物的功能性治愈带来了新的希望。
03、胜利曙光显现,小核酸药物能否率先冲线?
我们知道HBV会劫持肝细胞帮助其翻译蛋白质。
试想一下,如果没有这些RNA转录物,那么自然就无法继续产生乙肝病毒,其对免疫系统的压制也就不复存在。所以,通过降解病毒转录产物或者沉默其表达也就成为了抑制HBV的有效手段。
在多种小核酸药物中,反义疗法(ASO)和小干扰RNA(siRNA)已经产生了一定的效果,能够迅速降低HBV感染的指标。
先来说siRNA。siRNA是由细胞内双链RNA经酶复合加工产生,可以靶向切割特定的mRNA小片段,中断特定的mRNA翻译过程,从而抑制乙肝病毒复制。
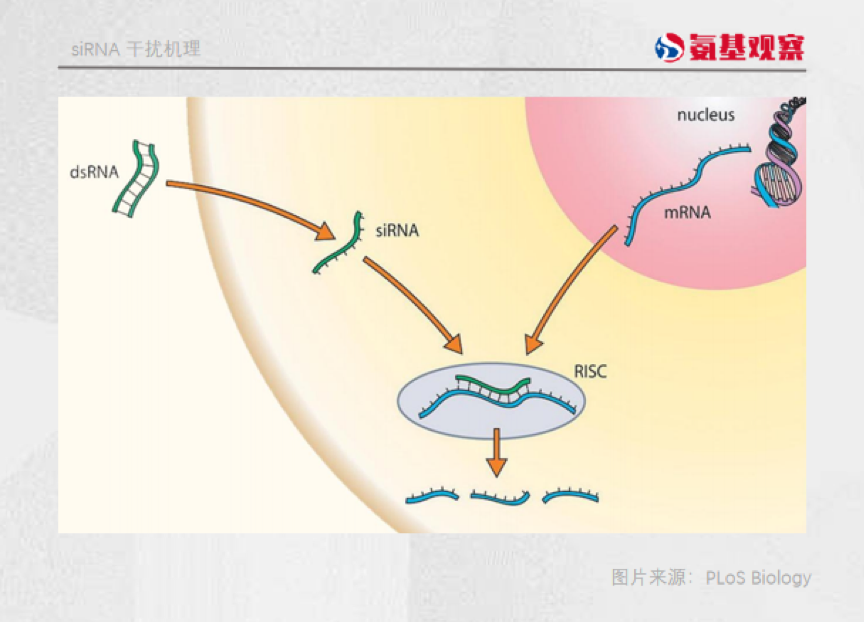
强生和ARWR共同研发的JNJ3989就是这样一款药物。最新公布的临床数据显示,JNJ-3989与核苷酸类似物联合使用,能够使得患者包括HBsAg在内的所有病毒标志物水平的持续下降。
在不少大药企看来,siRNA疗法将会成为乙肝治疗的基石,通过与核苷酸类似物、干扰素联合使用或许有望使乙肝达到功能性治愈。国内,腾盛博药正在和VIR合作研发siRNA乙肝药物。
不过,相比siRNA疗法,ASO药物或许抢先一步。
ASO主要通过碱基互补配对方式,与乙肝病毒的RNA结合,并募集肝脏自身的酶,将配对的乙肝RNA摧毁,最终使其失去活性。
葛兰素史克的ASO药物Bepirovirsen已经初步展现出了功能性治愈乙肝的潜力。
2022年6月末,Bepirovirsen公布了治疗慢性乙肝的临床Ⅱb期试验中期结果,主要终点是达到HBsAg水平低于量化下限(LLOQ)的患者比例。
结果显示,经过24周的治疗后,接受过核苷酸类似物治疗的患者中,HBsAg<LLOQ和HBVDNA<LLOQ的比例分别为28%,未接受过核苷酸类似物治疗的则为29%。
简单来说,24周的治疗后,近30%的乙肝患者HBsAg和HBV-DNA水平都低于可检测的*水平。
这一数据比目前的标准疗法效果要好得多,多项研究表明,在接受干扰素治疗的患者中,HBsAg的清除率为2.1%至20%,而核苷酸类似物的HBsAg清除率更低,随访2-7年后,HBsAg清除率为1.4-5.1%。
不过能Bepirovirsen能否真正成功,不到最后一刻谁也不敢妄下定论。
毕竟就在不久前,Aligos公司此前备受关注的ASO药物ALG-020572,因为严重不良事件而被迫停止。Bepirovirsen还处于临床二期,只有通过临床三期的考验才算成功。
但无论如何,Bepirovirsen好歹让人们看到了希望所在。
随着多种路径的乙肝治疗方式齐头并进,或许在不久的将来我们能看到乙肝患者能够真正实现功能性治愈。而率先冲线的药企,无疑也会获得丰厚的回报。
【免责声明】:本文不构成任何投资建议。市场有风险,投资需谨慎。
如有任何疑问,请联系(editor@zero2ipo.com.cn)投资界处理。












