将一头基因改造猪的肾脏连接到一位病人腹部外腿部的血管上,54 小时后撤下,其间猪肾过滤废物和排泄尿液的功能正常,没有产生排异反应——这是不久前,纽约大学医学院朗格医疗中心的医生所做的医学实验。医生表示,这一案例表明,猪肾可能成为透析患者以及终末期肾病患者的*选择。
在过去,大部分情境下,一名需要器官移植的病人能做的只有等待,最终能等到并且成功移植的,仅是其中非常小部分的幸运儿。
上世纪九十年代,以猪器官为主要目标供体的异种移植研究已经在业内出现,从开始的为人追捧,到后来面临技术困境,又因为伦理问题而被世卫组织禁止。近年来随着基因技术的进步,使得「基因改造猪」变得更加适合培养器官,纽约大学的此次试验也证明,时隔二十年后,异种器官移植或将迎来高速发展期。
「小猪配齐」,或许是未来又一大医疗风口。
01
「暂未产生排异反应」
接收者是一名脑死亡患者,有肾功能不全的迹象,经过协商,家属同意在为其移除维生仪器前参与试验。
那颗移植的肾脏来自美国联合治疗公司(United Therapeutics)的子公司 Revivicor 研发的一种科学家有意改变基因组的猪——GalSafe 猪。经过基因编辑,敲除了猪体内能催化细胞表面表达 α- 半乳糖(α-gal),即一种可能诱发人体排斥的糖分子的基因。
蒙哥马利(Robert Montgomery),美国纽约大学医学院朗格医疗中心的一名外科医生,将这颗猪肾脏,连接到了病人的腹部外腿部血管上。新肾脏附着在患者腿部血管上并保持在体外,盖有保护罩以便进行观察和肾组织取样。
54 个小时后,暂时没有出现受体免疫系统的排斥反应。研究者撤掉了受试者的呼吸机,标志着试验结束。
这次手术采用统称为在体灌流术的模型,蒙哥马利说,猪肾的功能看来相当正常,它制造的尿量,与移植人类肾脏所预期的尿量一样。病人原本异常的肌酐水平(Creatinine level,评估肾功能的指标),在接受猪肾移植后恢复正常。「来自逝者的肾脏往往需要数天到数周的时间才开始生效,而这个猪肾脏立即生效了。」
专家对此相当兴奋,「器官捐赠等待名单可能会立刻变得相当短。」
通常,异种器官移植导致的免疫排斥反应出现在人体血液供应与器官的交界处,但在此次手术中并未出现。
但在此次试验取得初步成功后,仍需要解决一些复杂的关键问题。基因编辑猪的肾脏虽然没有引起超急性排异反应(在器官移植 48 小时内发生的排异反应),但尚不知晓是否会产生加速性排异反应(48 小时至 5 天)、急性排异反应(1 周以上)和慢性排异反应。
此外,现在采用的基因编辑猪只是敲除了能催化半乳糖分子的基因,但猪器官内还隐藏着很多可能潜在引发人体免疫排异反应的物质,以及可能引起人患病的微生物,如猪身上特有的病毒等。
当然,此次实验的初步成功仍带来很多希望。在目前人体供肾不足的情况下,或许可以把这样的猪肾用于救治急性肾衰竭病人,短期内维持其生命,直到出现可用的人类肾脏,或把猪肾作为*性移植物,保留在体内。蒙哥马利医生说,基因工程猪「可能成为可持续、可再生的器官来源」。
目前,人体器官供不应求是世界性的难题。全世界每年约有 200 万人需要器官移植来治疗疾病,器官供者和受者的比例却不足 1:20。
肾脏的等待时间平均为三到五年,40% 的等待移植的患者可能在五年内死亡。据器官共享联合网络的数据,美国目前有近 107,000 人正在等待器官移植,其中超过 90,000 人正在等待肾脏移植。根据《中国器官移植发展报告(2019)》,截至 2019 年底,全国仍有 47382 人等待肾移植。
中国器官移植发展基金会理事长黄洁夫在 2020 年指出,目前中国每年因终末期器官衰竭而等待器官移植的患者约有 30 万人,每年器官移植数量却仅有约 2 万例。
02
「停滞的 12 年」
异种移植,指将一个物种的组织移植到另一个物种体内。和同种移植不同的是,异种移植成功的可能性很小。异种之间存在很大差异,负责组织排斥的免疫系统很容易识别出外来组织,并强烈排斥它。
相比与人类相似度更高的灵长类动物,猪产仔量多、生长快,因此维持成本较低,也不易引发伦理问题,且猪的器官和人的器官在大小和功能上均有非常相似的地方,多方面综合考虑,猪在人体器官移植等方面有着巨大的应用空间。
然而,由于先天免疫和炎症反应、凝血系统紊乱等安全问题以及猪器官本身携带病毒的危害性等问题,猪器官移植到人体的临床应用举步维艰。
科学家研究发现,猪器官移植引起排斥反应的主要原因是,人体内的天然抗体能识别出猪细胞表面的α-半乳糖苷酶(α-gal)、β-半乳糖苷酶(β-gal)和 N-乙酰神经氨酸羟化酶(Neu5Gc 蛋白),这 3 种蛋白分别由 GGTA1、B4GalNT2 和 CMAH 基因催化合成。只有将上述 3 个基因全部敲除,猪器官移植到人体后才几乎不会有大的排斥反应,才具有进入临床试验的基础。
本次手术中使用的肾脏便是通过敲除编码糖分子的猪基因获得的。
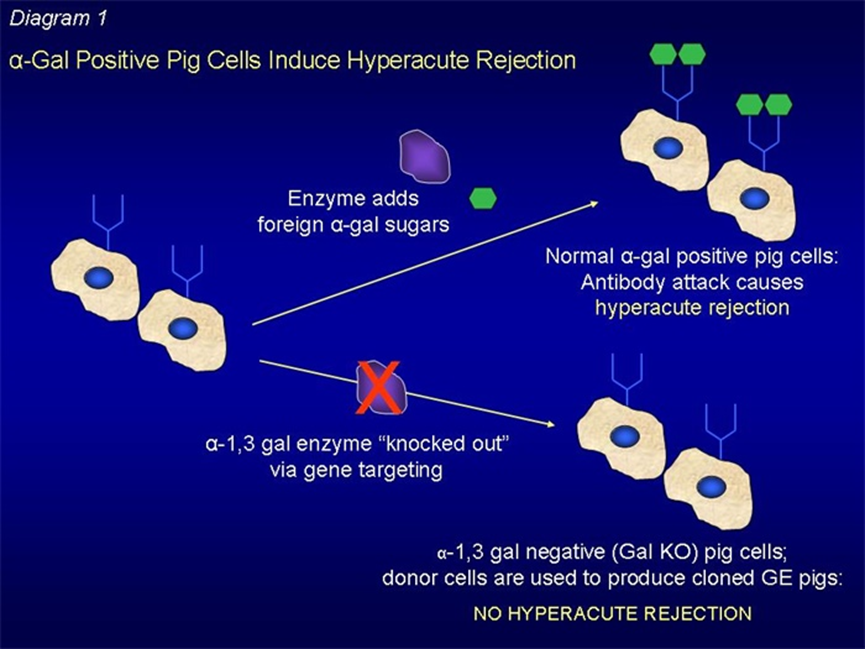
转基因猪实验逻辑,图源:Revivicor
上世纪 90 年代,猪器官移植项目曾一度在全球受到追捧,各大制药厂与企业致力于研发免除排异反应的药物,但是,猪器官移植到人体内不仅会产生免疫排斥反应,且猪基因里含有的逆转录病毒的序列对人也有潜在风险,因此,世界卫生组织明令,未找到解决方法之前,停止一切异种器官的临床试验。
2000 年,国际心肺移植协会提出,一旦 60% 移植了猪心脏的灵长类动物能够存活 3 个月,并至少有一定迹象表明其可以存活更长时间,就考虑在人身上试用猪心脏。
2003 年,美国 Revivicor 公司创造了世界上*只敲除α-Gal 糖分子基因的克隆猪。Revivicor 的前身是 PPL Therapeutics 生物技术公司——正是 PPL Therapeutics,在 1996 年培育出了*从成年哺乳动物克隆而来的哺乳动物:绵羊多利(Dolly)。
2018 年,《自然》的一篇报告指出,经过基因编辑的猪心脏移植到狒狒体内后正常存活 195 天。德国科学家选取幼年猪,基因修饰猪的心脏,将其移植到血压降至与猪一致的 5 只狒狒体内,手术成功,这意味着人类或许可以进行这样的器官移植试验。
杨璐菡是 eGenesis 公司的联合创始人与首席科学家。在哈佛大学攻读博士后期间,她和导师乔治·丘奇(George Church)首创了利用 Cripsr-Cas9 技术修改猪细胞基因组的做法,并在 2014 年开始了消除猪基因组中可能的致病基因的工作。
她说:「由于无法预期什么时候,以及用什么方法来解决这些问题,异种器官移植行业遭到了重创,经历了 12 年的停滞。」
2020 年 9 月,杨璐菡团队在《自然生物医学工程》上发表的论文表明其团队研发的第三代基因编辑猪(「猪 3.0」)已经获得成功,「猪 3.0」不但在免疫排斥方面有所突破,又敲除了内源性逆转录病毒(PERV)。「猪 3.0」细胞与人体凝血系统的兼容性更强,还减少了凝血的风险,可以延长移植器官的寿命。
2020 年 12 月,异种器官移植迎来了新的篇章。美国食品与药物监督管理局(FDA)批准了*可以同时用于人类食物消费和作为潜在疗法来源的转基因猪上市,即 Revivicor 研发的 GalSafe 猪。
也就是本次手术所用肾脏的供体猪。
03
一片巨大的「蓝海」
放眼全球,公开资料可查的异种器官移植公司总体数量并不多。
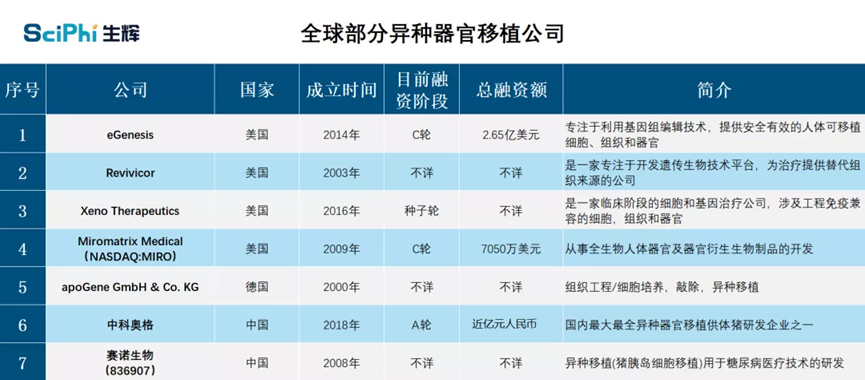
图源:生辉
eGenesis 作为启函生物的姊妹公司,是其中知名度最高的公司之一。今年 3 月,该公司宣布完成了 1.25 亿美元的 C 轮融资,用于推进在肾脏和胰岛细胞移植方面的主要项目,优化现有的基因编辑平台和 GMP 厂房。该公司正在创造三种猪的模型,并对基因工程器官进行有效性和安全性测试,预计 2022 年将开始进行临床试验。
而在手术中所用猪肾的猪是由 Revivicor 公司进行基因工程改造的。Revivicor 是全美少数几家致力于开发猪器官,以移植到人类身上的生物技术公司之一。去年 12 月,FDA 批准了 Revivicor 猪的基因改造,可用于人类食品和药物制造。目前,这家公司拥有 100 多头基因改造后的猪,用于移植试验与其他药物研究。
致力于使用猪器官进行人体异种移植的 Miromatrix Medical 公司今年 6 月在纳斯达克上市,成为*上市的异种器官移植公司。预计 2022 年底,该公司将开始对其生物工程肝脏进行有外部肝脏辅助系统支持下的人体临床试验。该公司已经开发出灌注去细胞化和再细胞化方法,能够将废弃的猪器官转化为可移植的人体器官。
国内方面,定位为「未来器官工厂」的中科奥格生物科技有限公司,正通过基因编辑与克隆技术培育了十余种基因修饰的人源化猪,用于异种移植研发,解决临床移植器官短缺问题。今年 9 月,该公司已完成 4500 万元 A 轮融资,目前正在筹建超洁净级猪设施(DPF)医用级异种移植医用供体基地,为临床试验做准备。
赛诺生物则致力于异种移植对糖尿病医疗技术的突破,其从培育的供体猪体内提取胰腺,制备猪胰岛细胞生物制剂,移植入患者体内特定部位 (以肝脏为主),为糖尿病患者重新构建较完整的胰岛系统,用于治疗 1 型糖尿病、有胰岛素依赖的 2 型糖尿病和因各种原因行胰腺全切除术后的患者。
异种器官移植是一个新兴的、巨大的、未被满足的市场,具有极大医疗潜力与商业价值,不少国内外企业已率先入局这一蓝海;科学家们正以精密的试验与先进的技术为支撑,为病人们争取一个摆脱焦灼煎熬与等待的未来。
器官采购组织 LiveOnNY 的首席医疗官艾米·弗里德曼博士说:「这是真正前沿的转化手术和移植,一旦成功了,想想我们可以提供多少移植物,真是令人难以置信!」












